Hey Leute,
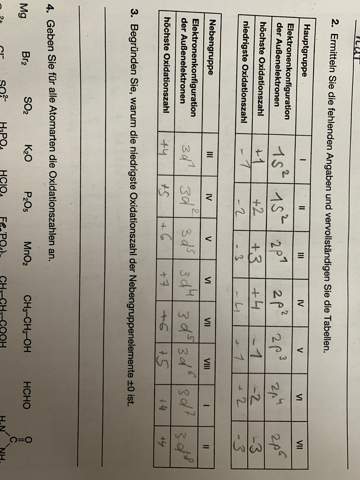
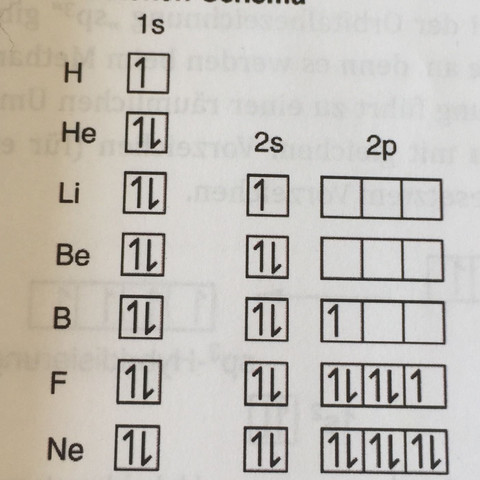
für die Elektronenkonfiguration von Fe2+ ergeben sich mir zwei Möglichkeiten: 1. [Ar] 4s0 3d6, da aus der äußersten Schale zwei Elektronen entfernt werden. 2. [Ar] 4s1 3d5, wie bei 1., doch nun gleichen sich laut der Pauli Regel noch die Elektronen so aus, dass es nur halbbesetzte Orbitale gibt. Eigentlich müsste doch 2. stabiler und damit häufiger sein, oder? Lese im Internet aber auch sehr oft 4s0 3d6, also wo ist der Haken, oder existieren vielleicht beide in einem bestimmten Verhältnis?
Vielen Dank schon im Voraus :)
Euer Gugstduu10