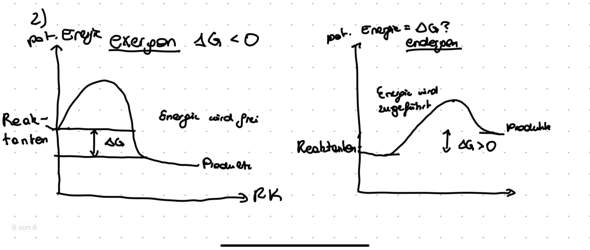
Wasser geht bekanntlich ein Autoprotolysegleichgewicht ein - es handelt sich um eine Umkehrreaktion der Neutralisationsreaktion, bei der 2 mol Wasser zu jeweils 1 mol Oxonium-Ione und 1 mol Hydroxid-Ione reagieren: H2O + H2O —> H3O+ + OH- (Enthalpie > 0, also endotherme Reaktion)
Bei 25°C beträgt die Konzentration c( H3O+)=c(OH-)= 10-7 mol · l-1, weshalb der pH-Wert dementsprechend 7 ist...
Wenn ich jedoch die Temperatur erhöhe, so nimmt der pH-Wert ab bzw. mein Wasser wird sauerer (Wichtig! Ich betrachte reines Wasser, ohne Beimischung von Säuren oder Basen).
Anfangs ist die Abnahme des pH-Wertes logisch, durch die Temperaturerhöhung verschiebt sich das Autoprotolysegleichgewicht zugunsten der Protolyse bzw. Produkte => es werden mehr Oxoniumione gebildet, somit steigt die Konzentration von c( H3O+) und der pH-Wert nimmt ab. Da die Protolyse jedoch Oxonium-Ione und Hydroxid-Ione im Verhältnis von 1:1 bildet, steigt doch analog dazu auch die Konzentration von c(OH-) an, was den pH-Wert erhöht bzw. die Abnahme des pH-Wertes entgegenwirkt..... Wieso ist es trotzdem so, dass der pH-Wert von Wasser abnimmt??