Wie Haworth zu Fischer umwandeln?
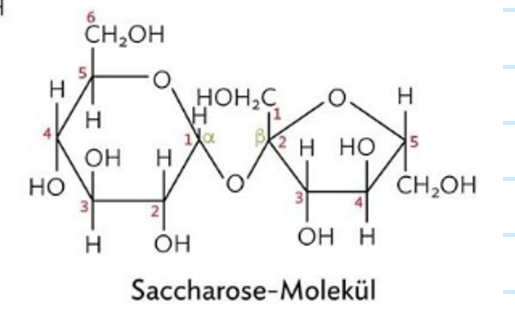
Ich habe dieses Saccharose-Molekül und soll jeweils die Stukturformeln der Monosaccharide zeichnen, aus denen es besteht.
Das linke verstehe ich, aber das rechte Molekül (welches Fructose sein dürfte?) verwirrt mich. Es ist, anders als normal in der Haworth-Projektion, nicht mit dem C1 rechts sondern mit dem C1 links dargestellt.
Man folgt normalerweise ja der Regel, was bei Haworth oben ist, ist bei Fischer links. Jetzt ist am C3 das H oben - müsste in Fischer also links sein. Danach kämen der Regel folgend eine Hydroxy-Gruppe links (am C4) und ein H-links (am C5).
Damit wären also am C2 die OH Gruppe rechts (weil CH2OH oben ist), am C3 wäre OH ebenfalls rechts (weil H links ist), am C4 wäre OH links und am C5 wäre OH rechts.
R-R-L-R ist aber nicht die Verteilung, die die Hydroxygruppen im D-Fructose-Molekül (OH Gruppe am letzten chiralen C ist rechts, daher D-Fructose) haben.
Sondern es müsste eigentlich R-L-R-R sein (beginnend an C1).
Da das so nicht sein kann, frage ich mich, wie ich richtig vorgehen sollte?
2 Antworten
Die Fructose bindet sich nun mal über das C2 an die Glucose. Wie willst du dann das C1 rechts zeichnen?
Aus Fischer links -> Hayworth oben wird dann halt Fischer links -> Hayworth unten. Oder anders, beim Übergang Fischer -> Hayworth wird das Molekül normal auf die rechte Seite gelegt, in diesem Fall auf die linke.
Wer sagt, dass es die Fischer-Projektion sein muss?
Spalte die glycosidische Bindung, ergänze H und OH, fertig.
Die Aufgabe verlangt die FIscher-Projektion, da diese den strukturellen Aufbau des Moleküls eindeutig anzeigt. Wenn man den Ring nicht richtig umschreibt, kann man in der offenen From sonst doch nicht mehr erkennen, um welchen Zucker es sich genau handelt, oder verstehe ich es falsch?