Formalladung hier richtig?
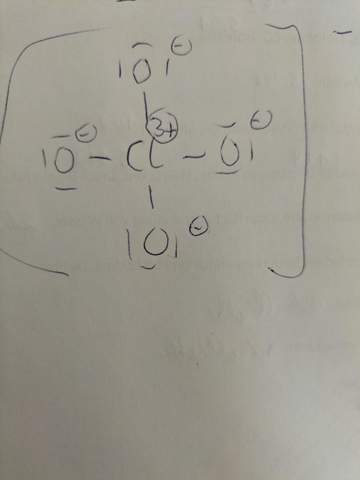
Ist das richtig?
2 Antworten

Das ist nicht richtig. Richtiger für das Perchlorat-Anion ist folgende Darstellung:
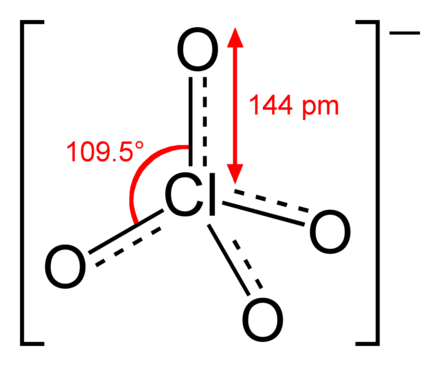
Dabei sind die jeweils freien Elektronenpaare an den Sauerstoffatomen weggelassen worden. Die Darstellung soll verdeutlichen, dass alle Sauerstoffe gleichartig sind und die Cl-O-Bindungen gleichen Anteil an Doppelbindungscharakter haben. Die Oxidationszahl (OZ) des Chlors ist hier +VII. Die 4 Sauerstoffe liefern 4 * -II = OZ -VIII. Die Differenz der OZ ist die Ladung des Ions mit einer negativen Ladung.
Oder vielleicht ist diese Darstellungsform eher dass, was in der Schule erwartet wird:
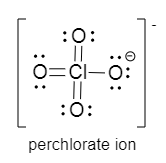
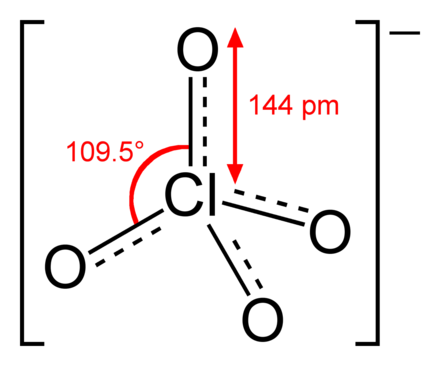
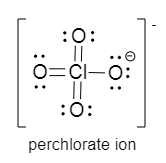

Ja, das passt.

Wohl ist mir dabei auch nicht, aber wenn man an der Oktettregel festhält, sind die Formalladungen richtig, und danach war gefragt.


Ich hatte die erweiterte Version mit Mehrfachbindungen schon angefangen, aber bin zur Ansicht gelangt, dass die eher verwirrt.
Ein wenig Schnuppern in einem PC-Buch hat zur Erkenntnis geführt, dass diese Verwirrung auf Schulniveau auch nicht entwirrt werden kann. Es sind da hybridisierte sp-p-sp-Sigma-Dreizentrenbindungen im Spiel, und von der Bindungsordnung bleibt es bei 4.

Nun ich meine eher die Darstellungsart mit 4 geladenen Sauerstoffatomen und einem 3-fach positiv geladenen Chloratom sieht für mich doch sehr exotisch aus. Macht man das heute in der Schule so?
Auch wenn ich es auf Schulniveau nicht besser darstellen kann - wohl ist mir nicht bei solcher Ladungstrennung.