Hey,
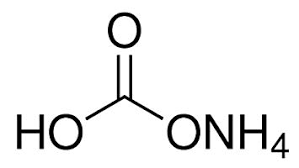
ich habe mich über das Salz Ammoniumhydrogencarbonat(Hirschhornsalz) beschäftigt und ich frage mich, wie eine solche Bindung '-ONH4'(rechts) entstehen kann?
Das Komische ist nur, dass das Sauerstoff genau 2 Bindungen mit einem anderen Atom haben sollte, um eine neutrale Ladung zu haben. Da das Sauerstoff eine Bindung zum Kohlenstoff-Atom schon hat, müsste die andere Bindung zum Stickstoff sein. Aber um, das Stickstoff, wie hier neutral zu halten, müsste es ingesamt 3 Bindungen haben. Eine Bindung ist schon grad an das Sauerstoff vergeben. Dann bleiben uns nur noch 2 Bindungen, die noch von zwei Wasserstoff- Atomen gefüllt werden. Trotzdem bleiben dann von den vier Wasserstoffatomen, zwei Atome ohne Bindung zum Molekül übrig.
Wie ist es dann diese Schreibweise möglich, wenn die Bindung vom NH4+ und O- nicht funktioniert? Ich finde die Ionenform viel plausibler. Kann jemand mir erklären, wie diese Form bitte zu Stande kommt?
Ich freue mich auf auf Antworten. LG, Julius