Wie kann eine '-ONH4'-Bindung entstehen und wie würde sie dann aussehen?
Hey,
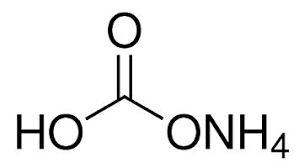
ich habe mich über das Salz Ammoniumhydrogencarbonat(Hirschhornsalz) beschäftigt und ich frage mich, wie eine solche Bindung '-ONH4'(rechts) entstehen kann?
Das Komische ist nur, dass das Sauerstoff genau 2 Bindungen mit einem anderen Atom haben sollte, um eine neutrale Ladung zu haben. Da das Sauerstoff eine Bindung zum Kohlenstoff-Atom schon hat, müsste die andere Bindung zum Stickstoff sein. Aber um, das Stickstoff, wie hier neutral zu halten, müsste es ingesamt 3 Bindungen haben. Eine Bindung ist schon grad an das Sauerstoff vergeben. Dann bleiben uns nur noch 2 Bindungen, die noch von zwei Wasserstoff- Atomen gefüllt werden. Trotzdem bleiben dann von den vier Wasserstoffatomen, zwei Atome ohne Bindung zum Molekül übrig.
Wie ist es dann diese Schreibweise möglich, wenn die Bindung vom NH4+ und O- nicht funktioniert? Ich finde die Ionenform viel plausibler. Kann jemand mir erklären, wie diese Form bitte zu Stande kommt?
Ich freue mich auf auf Antworten. LG, Julius
4 Antworten
Es handelt sich um ein Salz. Deine Darstellung also falsch, man darf das N nicht direkt neben das O schreiben, und einen Bindungsstrich darf man erst recht nicht zeichnen.
- Das Kation ist Ammonium NH₄⁺. Hierin hat der Stickstoff ausnahmsweise 4 Bindungen. Für eine stellt er sein normal freies Elektronenpaar zur Verfügung.
- Das Anion ist das Hydrogencarbonat. Bei dem ist 1 O-Atom einfach gebunden und hat 3 freie Elektronenpaare und damit eine negative Ladung. Rein formal, in Echt teilen sich die beiden O-Atome, die kein H gebunden haben, sowohl die Doppelbindung als auch die negative Ladung. Nennt sich Mesomerie.
Zwischen den Ionen gibt es nur elektrostatische Anziehung, keine Atombindungen.
Hallo SuperJulius
Ich weiß nicht, woher du diese Formel hast. Korrekt müsste sie nämlich so aussehen:
https://upload.wikimedia.org/wikipedia/commons/1/14/Ammonium_bicarbonate.png
Ammoniumhydrogencarbonat ist ein Salz:
NH₄HCO₃ → NH₄⁺ + HCO₃⁻
Es liegen Ionen in Ionenbindung vor.
LG
Ich habe mich auch deshalb gewundert, wie es funktionieren kann.
Da es ein Salz ist, enthält es Ionen!
NH4+ (Ammonium) ist das Kation von Ammoniak und der Sauerstoff hatte vorher ein positivierten Wasserstoff als Proton ans Wasser abgegeben und bleibt als negatives O=C-O- (Carboxylat) Anion zurück. Dann ziehen sich positiv und negativ an (Coulomb Gesetz).
Das ist doch auch ionisch aufgebaut, also Anion der Carbonsäure und Kation NH4+