Woher weiß man ob bei Salzen nur eine Wertigkeit auftreten kann?
Ich kann da keine Regelmäßigkeit erkennen, wann es angegeben wird und wann nicht.
Weiter oben im Text heißt es:
Bei Metallen, die Kationen mit unterschiedlicher Ladung bilden, wird die Ladung durch eine römische Zahl angegeben (entsprechend der Oxidationszahl), die in Klammern dem deutschen Namen des Metalls folgt:
Fe2+ = Eisen(II)-ion
Fe3+ = Eisen(III)-ion
Wenn das Kation nur in einer Wertigkeit auftreten kann, entfällt die Angabe der Wertigkeit.
Beispiel für Salz mit Kation einer Wertigkeit: KNO3 (Kaliumnitrat)
(und woher weiß man das?)
Name des Salzes:
Wenn es nur eine Möglichkeit einer Salzbindung zwischen zwei Elementen gibt, entfällt die Angabe der Wertigkeit (Oxidationszahl) des Metall-Ions: Natriumchlorid NaC
Ich check jetzt nicht, warum man es sowohl bei Chlorid als auch bei -oxid dann doch manchmal angibt.
Daran, ob das Kation aus ner Nebengruppe kommt oder nciht kann es ja nicht liegen...
4 Antworten
Welche Metalle in verschiedenen Wertigkeiten vorkommen, und welche die häufigsten sind, muss man sich merken.
Und wie du richtig erkannt hast, ist die Wertigkeit auch bei Hauptgruppenmetallen variabel. Da ist es aber etwas einfacher, bei denen gibt es noch eine Wertigkeit 2 niedriger als die maximale, die bei schwereren Elementen wichtiger wird. So treten sowohl Sn als auch Pb 2- und 4wertig auf, aber bei Sn ist +4 stabiler, bei Pb +2. Bei Bi ist entsprechend +3 stabiler als +5.
Bei den Nichtmetallen muss man nichts weiter angeben, weil der Name schon alles sagt. "Oxid" bedeutet immer OZ -2, sonst hieße es Peroxid, Hyperoxid, Ozonid. Chlorid hat immer die OZ -1.
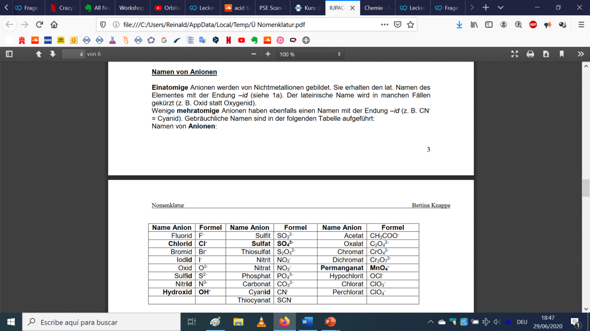
Siehe auch deine Liste der Anionen. Die muss man sich einprägen. OK, Thiocyanat und Oxalat vielleicht nicht unbedingt. Aber unbedingt mit Ladung.
Natriumchlorid ist also eindeutig, weil da "chlorid" steht und Na "immer" OZ +1 hat.
Bei den Anionen meinte ich die Liste, die du als letztes Bild hast. Klar ist die nicht vollständig.
Wenn du Metalle meinst, dann stehen die wichtigsten OZ bei Wikipedia. Soweit ich weiß, stehen sie auch in Vielen PSEs.
Eigentlich brauchst du aber nur die kennen, die im Unterricht drankommen, Kationen wie Anionen.
Die Wertigkeit gibt man bei Metallen an, die in einer Nebengruppe stehen, da diese unterschiedliche Wertigkeit haben können. Metalle in Hauptgruppen haben immer die gleiche Wertigkeit, deshalb braucht man die Angabe nicht.
aber guck mal, Zn ist Nebengruppe und es wird weggelassen
Pb und Bi sind Hauptrguppe und werden angegeben
Im s-Block ist es einfach: Alkalimetalle kommen fast immer in der Oxidationsstufe +I vor (Wasserstoff gelegentlich aber auch −I), Erdalkalimetalle haben so gut wie immer +II.
Der p-Block ist etwas komplizierter: Die Metalle und viele Halbmetalle haben gewöhnlich die Wertigkeit ihrer Gruppennummer, z.B. Al(III), Ge(IV), die schweren (5p, 6p) bevorzugen aber gewöhnlich die Oxidationszahl Gruppennummer minus Zwei, zB. Bi(III), Pb(II). Die Nichtmetalle können in so gut wie jeder Oxidationszahl zwischen der Gruppennummer und der Gruppennummer minus Acht auftauchen, gewöhnlich in Zweierschritten.
Bei den Übergangsmetallen bis Du aber mit Faustregeln am Ende. Für die frühen Vertreter (bis zur Eisengruppe) gilt, daß die maximale Oxidationszahl von links nch rechts wächst, also Sc(III), Ti(IV), V(V), Cr(VI), Mn(VII); Eisen sollte also die maximale Oxidationszahl VIII haben, tut das aber nicht (bei seinen schweren Homologen Ru und Os gibt es diese Stufe aber wirklich).
Die leichten Vertreter (also 3d) treten gerne mit Oxidationszahl +II oder +III auf, die schwereren (4d und 5d) bevorzugen dagegen höhere Oxidationszahlen.
In der Kupfergruppe ist alles möglich, auch die sonst seltene Oxidationszahl +I; dafür ist es bei der Zinkgruppe einfach, die treten überwiegend als +II in Erscheinung (nur Quecksilber mag manchmal auch +I).
Ich check jetzt nicht, warum man es sowohl bei Chlorid als auch bei -oxid dann doch manchmal angibt
Wo wird das "manchmal" angegeben?
Die Wertigkeit orientiert sich an dem Kation, die Nichtmetalle interessieren hier nicht, da spielt es es nur eine Rolle wie viel ich von dem Schrott brauche um die Gesamtladung auf 0 kriegen.
Pb und Bi sind Hauptrguppe und werden angegeben
Das ergibt auch Sinn, da die beiden Elemente verschiedene Wertigkeiten besitzen, da macht es keinen Unerschied ob sie in der Hauptgruppe stehen oder nicht.
Ich kann ja nicht einfach sagen: "Blei und Sauerstoff reagieren zu Bleioxid", wenn es unterschiede in der Wertigkeit von Blei gibt. Da ist das Erste was du darauf zu hören bekommst um was für ein Blei es sich in deiner Rede handelt.
Blei kommt in der Wertigkeit (II) und (IV) vor und daran orientiert man sich, ob der Verbindungspartner dabei Chlor, Sauerstoff oder der Nikolaus ist, das vollkommen egal und spielt keine Rolle.
Das Einzige was du bei Blei(II)-chlorid / PbCl2 und Blei(IV)-chlorid / PbCl4
herausliest ist die Anzahl der einzelnen Valenzelektronen, sprich wie Viel das Element bereit ist zu invenstieren in eine Bindnung und diese gilt es am Ende auszugleichen.
Tritt ein Element mit verschiedenen Wertigkeiten auf den Plan, dann wird diese entsprechend gekennzeichnet wie es auch bei Eisen oder Kupfer der Fall ist und das war auch schon alles was man dazu wissen muss.
Wo wird das "manchmal" angegeben?
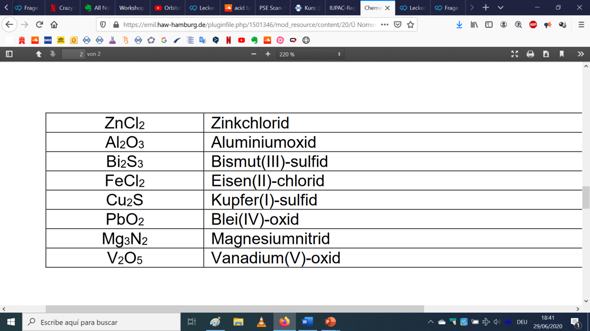
auf dem obersten bild wird es mal angegeben, mal nicht
Die Wertigkeit wird bei Bismut, Kupfer, Blei und Vanadium angegeben und das liegt daran, dass diese Elemente Unterschiede innerhalb ihrer Wertigkeiten haben.
Bismut tritt ebenfalls als Bismut(II) auf, Kupfer ebenfalls als Kuper(I) & Kuper(II), Blei als Blei(II) & Blei(iv), Vanadium als V(III), V(iv) und V(V).
Bei Eisen ist das ebenfalls der Fall, da Eisen nicht einfach Eisen ist, sondern als Fe(II) oder Fe(III) vorkommen kann.
Du machst es dir schwieriger als es in Wahrheit ist, die römische Zahl neben der Elementbezeichung signalisiert dir einfach gesagt in diesem Fall, dass dieses Element in diversen Wertigkeiten in der Natur vorliegt.
Warum darf man das zum Beispiel bei Zinkchlorid ignorieren?
Aus dem einfachen Grund, da Zink im Vergleich zu den oben genannten Elementen in keiner weiteren Wertigkeit als +3 vorkommt und ebenfalls weil Chemiker genau wie alle anderen Naturwissenschaftler faul sind und sich nicht die Mühe machen die Wertigkeit für jeden einzelnen Stoff aufzuzeigen, wenn es nicht absolut notwendig für das Verständnis ist.
Vergiss das mal schnell mit dem Chlorid und Oxid, denn das spielt hier keine Rolle, du betrachtest immer nur das Kation und nicht das Anion in der Verbindung, denn dieses gibt die Wertigkeit des Salzes vor.
Es wird doch bereits oben erwähnt
Wenn das Kation nur in einer Wertigkeit auftreten kann, entfällt die Angabe der Wertigkeit.
damit ist nicht gemeint, dass das Kation einfach positiv geladen sein muss, sondern, dass dieses nur in einer Wertigkeit auftritt wie es bei Zink, Magnesium und Aluminium der Fall ist.
hmm okay hast du ne ahnung wo man sone "auflistung" finden könnte?