E/Z- Isomere?
Ich sollte zu folgender Verbindung das entsprechende E-Isomer dazu zeichnen:
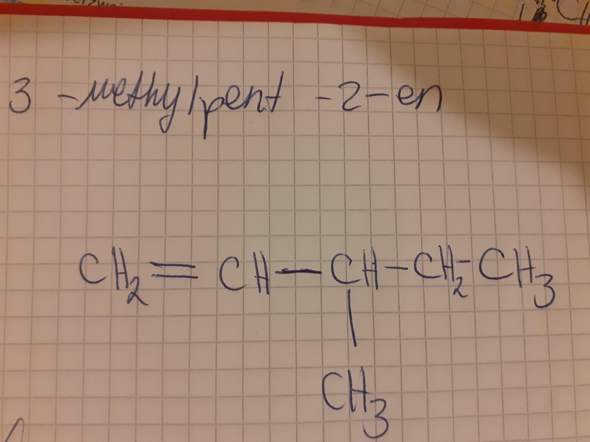
Aber wie komm ich jetzt auf das E-Isomer? Gibt es da eine Methode?
4 Antworten
Bei diesem Molekül gibt es keine Z/E-Isomerie, weil eines der beiden C-Atome an der Doppelbindung zwei gleiche Substituenten (in diesem Fall H) trägt. Entweder ist das eine Fangfrage, oder sie ist falsch gestellt (oder falsch abgeschrieben).
Allerdings ist das Molekül chiral und zeigt daher optische Isomerie, also gibt es eine S- und eine R-Struktur.
Ja hast es falsch gezeichnet. 2-en bedeutet, dass die Doppelbindung an Position 2 anfängt, nicht wie du gezeichnet hast aufhört. Dann wäre die Methylgruppe und das Ende der Doppelbindung am C3-Atom.
Nein, weil die Wertigkeiten/Prioritäten der Substituenten hier keine Rolle spielt bzw. auf einer Seite identisch sind (links bei H Atome)
Es gibt kein E/Z Isomere hier. Ich meine es so, wie ich es geschrieben habe
Aber mir ist aufgefallen, dass meine Zeichnung doch falsch ist.
Moin,
du hast (gemessen an der Überschrift) ein falsches Molekül gezeichnet.
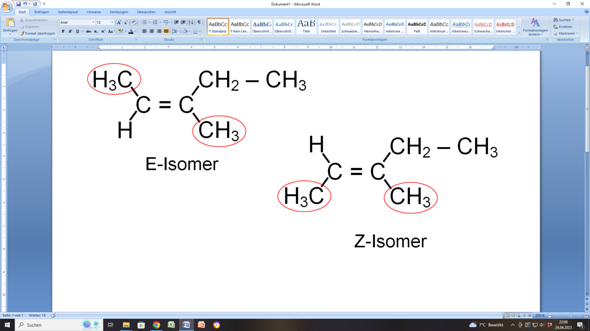
3-Methylpent-2-en sieht so aus:
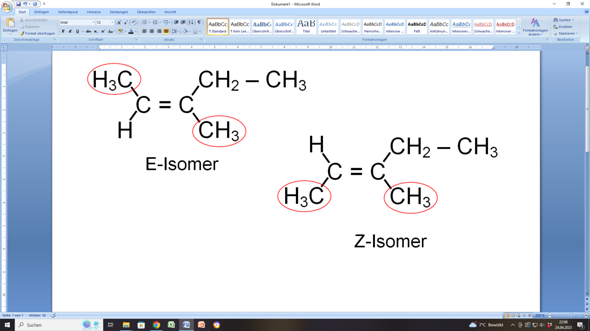
LG von der Waterkant
Wie sind die Regeln welche Substituenten man für die Bestimmung von E/Z anschaut? Ich habe gemeint, diejenigen mit der höchsten Priorität
Ach, ich hab es jetzt schon verstanden. Wenn man es richtig zeichnet ist es sehr eindach. Danke für deinen Hinweis, war schon wegen den vielen Antworten verwirrt.
Also gibt es keine Isomerie zu "3-Methylpent-2-en", vielleicht hab ich das auch falsch gezeichnet?