Hallo, ich habe eine Aufgabenstellung und ich komme dort gar nicht vorran :(.
Ich würde mich über Tipps freuen
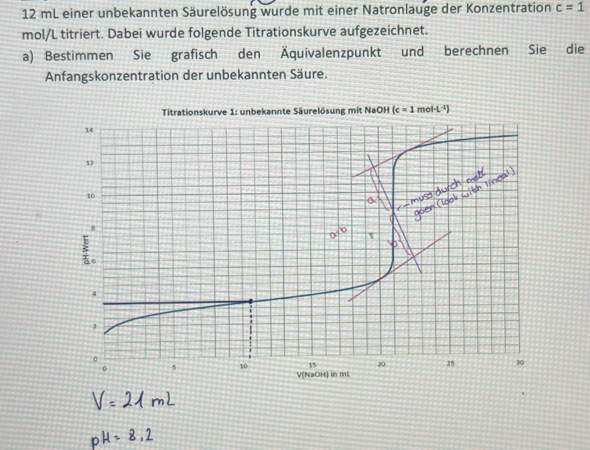
Titration: 20 mL einer 2,5 N Ammoniaklösung werden mit einer 5 N HCl titriert. Der pH-Wert wird mit dem pH-Meter verfolgt. Der pKB von Ammoniak beträgt 4,76.
a) Stellen Sie die Reaktiongleichung auf!
b) Welchen pH hat die Ammoniaklösung vor der Titration?
c) Nach welchem Volumen HCl wird der Pufferpunkt erreicht?
d) Welchen pH-Wert werden Sie am Pufferpunkt messen?
e) Nach welchem Volumen HCl wird der Äquivalenzpunkt erreicht?
f) Welcher pH herrscht rechnerisch am Äquivalenzpunkt?
g) Welcher pH-Wert wird nach Zugabe von 15 mL HCl gemessen?
h) Zeichnen Sie die Titrationskurve in ein Diagramm, bei dem die X-Achse dem verbrauchten Volumen HCl und die y-Achse dem pH-Wert entspricht.