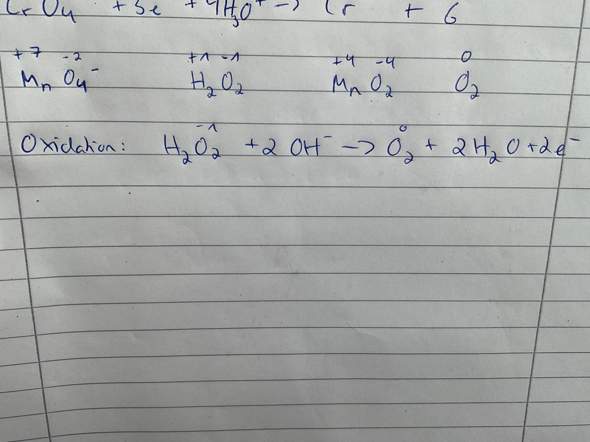ich habe folgende Produkte und Edukte gegeben. Beim Wasserstoffperoxid beträgt die Oxidationszahl für den Wasserstoff +1 und für den Sauerstofff -1. Bei der Oxidation werden dann zwei Elektronen auf der Produkt Seite hinzugefügt. Aber eigentlich gleichen sich die Oxidationszahlen von H und O doch aus und es ist 0. Dann würde zwar keine Oxidation zu O2 stattfinden, aber so würde es von den Oxidationszahlen für mich Sinn ergeben. Kann mir jemand erklären wieso man die Oxidationszahl vom Wasserstoff nicht beachtet? Und woher weiß ich, dass O hier -1 und nicht wie üblich -2 hat?