Wieso ist für die Titration von Ameisensäure mit Natronlauge nicht Bromphenolblau (3-5 pH) als Indikator geeigent?
2 Antworten
Von gutefrage auf Grund seines Wissens auf einem Fachgebiet ausgezeichneter Nutzer
Chemie, Naturwissenschaft, ph-Wert
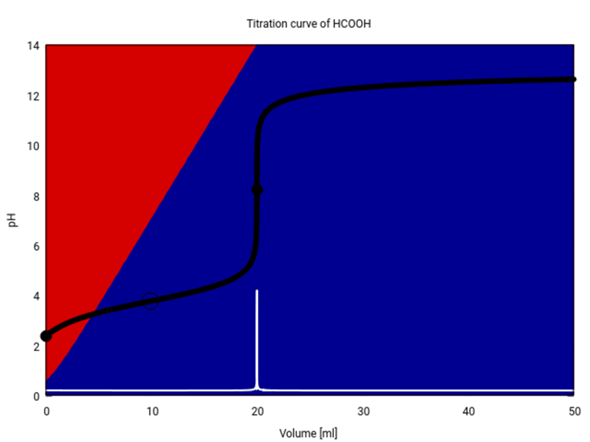
Die Titration sieht ungefähr so aus (20 ml Ameisensäure mit NaOH, beides 0.1 mol/l).
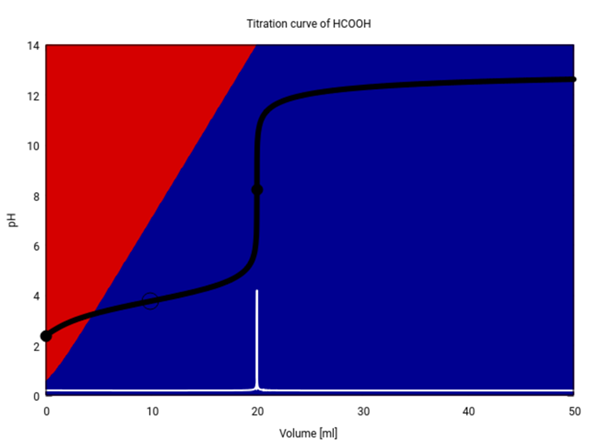
Der pH-Sprung liegt zwischen pH=5 und 11, also eher leicht alkalisch. Das liegt daran, daß Ameisensäure eine eher schwache Säure ist und daß daher das Natriumformiat (das am Äquivalenzpunkt rein vorliegt) schwach alkalisch reagiert. Du brauchst also einen Indikator, der so grob um pH≈8 umschlägt.
Woher ich das weiß:Studium / Ausbildung – Chemiestudium mit Diss über Quantenchemie und Thermodynamik
@lars675st
Fie letzte Frage hat sich geklärt,nur die erste Frage noch nicht:/
Von gutefrage auf Grund seines Wissens auf einem Fachgebiet ausgezeichneter Nutzer
Chemie
Welchen pH Wert erwartest Du denn bei einer NEUTRALISATION?
Woher ich das weiß:Studium / Ausbildung – MSc in Biochemie
Danke-ich hätte eine weitere Frage -ich soll erläutern (mit Rechnung), wie ich eine CalciumhydroxiLösung der Konzentration 0.01mol,100ml herstellen kann. In einem halben Liter sind 1.6g Calciumhydroxid gelöst.
Außerden verstehe ich nicht, wie ich auf die c der Calciumhydroxidlösung und die gelöste Masse komme, wenn sie mit HCL(0.1mol/l) titriert wird, und für 50ml Lösung 8ml HCl verbraucht werden