pKs/pKb?
Hallo, warum genau ist pKs+pKb eines konjugierten Säure-/Base-Paars 14?
Also: warum genau ist pKs+pKb=14?
Hier auf Gutefrage.net habe ich nur eine andere Frage gefunden welche in diese Richtung geht, jedoch war die Antwort für mich nichtsaussagend, bzw. ich habe es nicht verstanden.
2 Antworten
Ich habe das schon einmal genau erklärt: https://www.gutefrage.net/frage/warum-ist-pkspkbpkw-14#answer-515993484
Wenn das die Antwort ist, die Du nicht verstanden hast, dann frag nach. Aber hier die Kurzform: Die Säure/Basen-Konstanten beschreiben die Reaktionen
CH₃COOH + H₂O ⟶ CH₃CO₂¯ + H₃O⁺ Gleichgewichtskonstante Ka
CH₃CO₂¯ + H₂O ⟶ CH₃COOH + OH¯ Gleichgewichtskonstante Kb
Jetzt berechnen wir das Produkt der beiden Konstanten, dabei kürzt sich das meiste weg (weil die Summe der beiden Reaktionen nur die Autoprotolyse des Wassers ist)
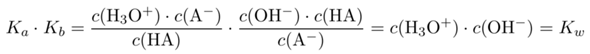
und nach dem Logarithmieren bekommt man
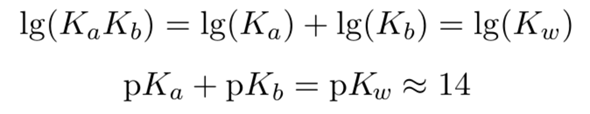
weil pKₐ = −lg(Kₐ) etc.
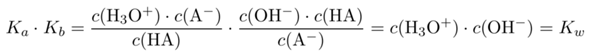
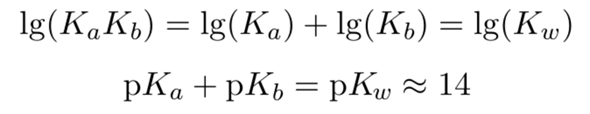
Weil in wässrigen Lösungen immer [H3O+] x [OH-] = 10-14 mol²/l² ist (Ionenprodukt des Wassers). Diese Gleichung wird auf der linken und rechten Seite logarithmiert und die Logarithmen mit -1 multipliziert. Statt -lg schreibt man dann p.
dann lautet die Gleichung:
lg[H3O+] + lg [OH-] = -14 ; / x (-1)
- lg[H3O+] - lg [OH-] = 14;
p[H3O+] + p[OH-] = 14 ;