Berechnung mit der Nernst-Gleichung?
Berechne die Spannung von diesem galvanischem Element:
Zn|Zn2+(0.05mol/l) // Br2|2Br-(0.1mol/l)

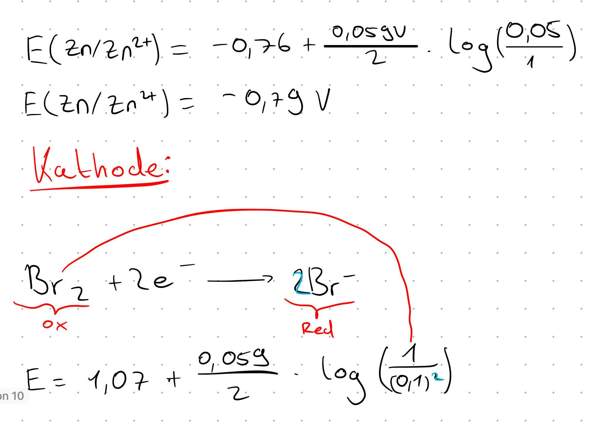
Bei der Gleichung mit der Zink-Halbzelle wird die Konzentration des reduzierten Stoffes auf 1mol/l gesetzt so wie es bei allen Feststoffen der Fall ist.
Aber warum ist es bei der Brom-Halbzelle andersrum und warum wird der Faktor vor dem Bromid-Ion innerhalb der reduzierten form zum Quadrat genommen. Ist das eine Regel für alle nicht-festen Stoffe?
3 Antworten
Ich denke mal, hier wird einfach angenommen, dass du einen Überschuss deiner Edukte hast und das ganze im wässrigen Medium stattfindet, also Bromwasser verwendet wird. Da sich Brom nur schwer in Wasser löst, hast du quasi eine konstante Konzentration von Br2, weil alles was abreagiert wieder nachgeliefert wird (also vom nicht gelösten Brom, das sich im Wasser absetzt). Damit kannst du die Br2 Konzentrarion auf 1 setzen wie beim festen Zn. Das Bromid Br- löst sich aber im Wasser, da spielt die Konzentration also eine Rolle (die hast du ja auch gegeben).
Das Quadrat beim Br- kommt aus der Reaktionsgleichung (du machst aus Br2 -> 2 Br-) bzw aus dem Massenwirkungsgesetz. da setzt du die Koeffizienten aus den Reaktionsgleichungen als Potenzen der Konzentrationen. Und nichts anderes ist das hier. Der ln bzw log aus der Nernstgleichung kommt nämlich aus dem Massenwirkungsgesetz. Da steht also ...+ 0,059 V/z * log(K).
Die Nernst-Gleichung berechnet die Elektropotentialspannung einer Halbzelle (Zink- oder Brom-Halbzelle in diesem Fall). Bei der Zink-Halbzelle wird die Konzentration des reduzierten Stoffes (Zink-Ion) auf 1 mol/L gesetzt, weil Zink als Feststoff vorliegt und seine Konzentration konstant ist.
In der Brom-Halbzelle bezieht sich der Faktor vor dem Bromid-Ion auf dessen Aktivität, die von der Konzentration abhängt. Die Aktivität wird immer mit dem Faktor multipliziert, um die effektive Konzentration zu berechnen. Da Brom als Lösung vorliegt, ist seine effektive Konzentration nicht konstant und hängt von der Konzentration ab.
Das Quadrieren des Faktors vor dem Bromid-Ion innerhalb der reduzierten Form ist eine Regel für Elektrolytlösungen. Es berücksichtigt die Dopplung der Ladung, die bei der Elektrolyse stattfindet.
Zusammenfassend ist es wichtig zu beachten, dass die Nernst-Gleichung anwendbar ist, wenn ein Elektronentransport stattfindet und die Konzentrationen von Elektrolytlösungen und/oder Aktivitäten berücksichtigt werden müssen.
In der Zink-Halbzelle wird die Konzentration des reduzierten Stoffes (Zn) auf 1mol/l gesetzt, weil Zink ein Feststoff ist und seine Konzentration im Gegensatz zu Lösungen nicht variiert werden kann.
In der Brom-Halbzelle hingegen wird die Konzentration des oxidierten Stoffes (Br2) auf einen bestimmten Wert (0.1mol/l) gesetzt, weil es sich hierbei um eine Lösung handelt und die Konzentration des Broms variiert werden kann.
Der Faktor vor dem Bromid-Ion (2) innerhalb der reduzierten Form wird zum Quadrat genommen, weil jede Brommolekül 2 Bromid-Ionen (Br-) beinhaltet. Daher wird die Anzahl der Bromid-Ionen, die an der Reaktion beteiligt sind, durch das Quadrieren des Faktors 2 ausgedrückt.
Das ist keine Regel die für alle nicht-festen Stoffe gilt, sondern es ist eine spezifische Anforderung für die Brom-Halbzelle. Jede Halbzelle hat ihre eigenen Anforderungen und Regeln, die befolgt werden müssen, um die Gesamtspannung (EMK) einer Zelle zu berechnen.