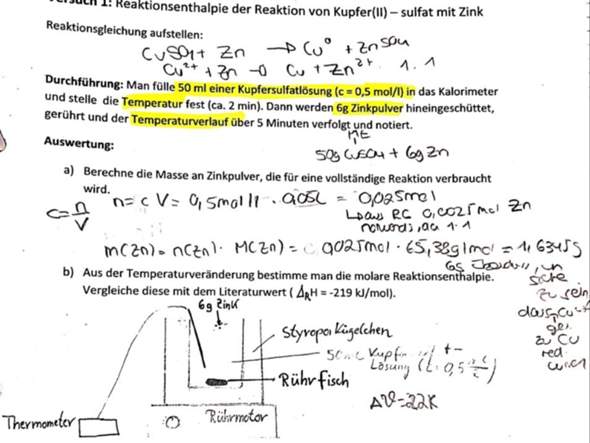
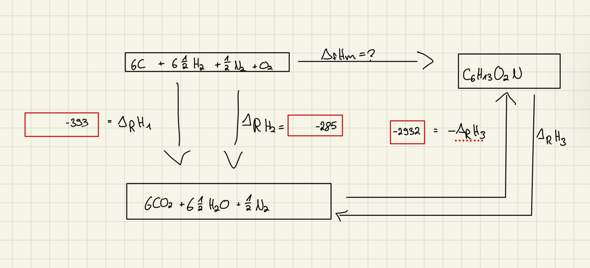
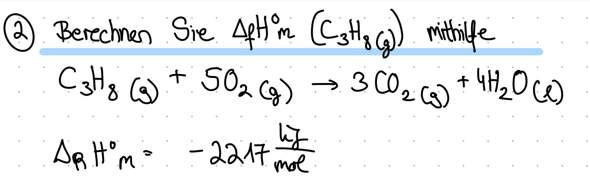
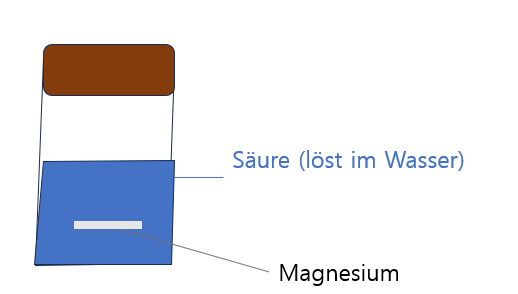
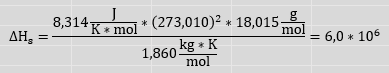Hallo, ich schreibe bald eine Chemieklausur und habe ein Verständnisproblem (zum Thema Enthalpie)
Zum Beispiel entspricht die Enthalpie (Delta H) der bei konstantem Druck gemessenen Reaktionswärme. Dann gibt es noch die Formel der Reaktionswärme, nämlich wird die mit folgender Formel berechnet: Qr = Cp • m • delta T .
Die Formel der Enthalpie ist Delta H = Delta U + p • Delta V. Also irgendwie ist beides die Reaktionswärme, da die Enthalpie als solche definiert ist.
Dies würde doch bedeuten, dass die Reaktionswärme das Gleiche ist wie die Enthalpie. Was mache ich, wenn nach der Enthalpie gefragt ist? Berechne ich diese mit der Formel Qr = (...) oder mit Delta H = (...) ? Einerseits berechnet man mit einer Formel die Reaktionswärme (Qr = Cp • m • Delta T), aber andererseits gibt es noch die andere Formel für die Reaktionswärme (in dem Fall die Enthalpie )(Delta H = Delta U + p • Delta V). Ich hoffe man versteht das Problem. Worin liegt der Unterschied von Qr = Cp • m • delta T zu Delta H = Delta U + p • Delta V ?
Ein ähnliches Problem habe ich, wenn nach der Reaktionsenthaplie gefragt ist. Berechne ich diese mit der Formel der Standart-Bildungsenthalpie oder mit der Formel der Reaktionswärme oder mit der Enthalpieformel?
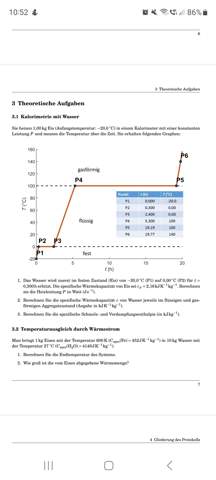
Im Anhang sende ich noch meine Notizen, vielleicht könnt ihr mir helfen. Ich habe so viel gelesen, dass ich leider ziemlich durcheinander gekommen bin.