Wie ein Schalenmodell für ein Molekül zeichnen?
z.B. Schalenmodell für ein Sauerstoff-Molekül.
Was muss ich vom Periodensystem dafür ablesen bzw was kann man (für ein Schalenmodell für Moleküle) nützliches vom PSE ablesen?
3 Antworten
Moin,
dir muss klar sein, dass ein Molekül mit mindestens einer Atombindung nach einer Faustregel zwischen mindestens zwei Nichtmetallatomen zustande kommt.
Dann kannst du anhand eines (guten) PSE sehen, welche Elemente dafür in Frage kommen.
Außerdem kannst du am PSE ablesen, wie viele Außenelektronen (Valenzelektronen) die Atome der betroffenen Elemente haben. Hier gilt: Hauptgruppennummer = Anzahl der Valenzelektronen.
An der Periode erkennst du, wie viele Schalen überhaupt mit Elektronen besetzt werden müssen. Je nach Stellung des Elements ergibt das für die Elemente...
- ... Wasserstoff: eine Schale
- ... Bor, Kohlenstoff, Stickstoff, Sauerstoff und Fluor: zwei Schalen
- ... Silicium, Phosphor, Schwefel und Chlor: drei Schalen
- ... Selen, Brom: vier Schalen
- ... Iod: fünf Schalen
Je nach Stellung des jeweiligen Elements musst du verschieden viele Elektronen in die dritte Schale malen:
- Silicium, Phosphor, Schwefel und Chlor haben 8 Elektronen in der 3. Schale
- Selen, Brom und Iod haben 18 Elektronen in der 3. Schale
- Iod hat dann auch noch einmal in der 4. Schale 18 Elektronen
Dann kannst du mit Hilfe der Oktettregel darauf kommen, wie viele Atombindungen ausgebildet werden müssen, damit alle beteiligten Bindungspartner ihre Außenschale mit Elektronen voll bekommen (Wasserstoff braucht dazu 2 Elektronen, die anderen 8 Elektronen).
Und dann musst du das nur noch geschickt aufmalen.
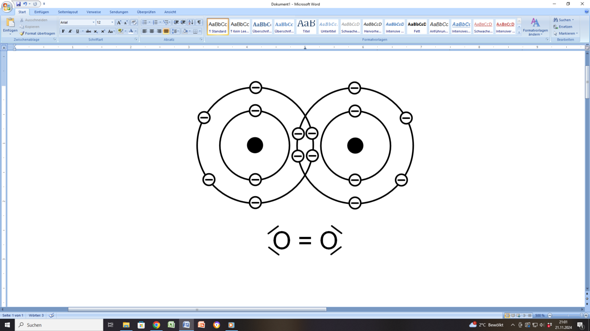
Für das Sauerstoff-Minimoleküle zum Beispiel so:

Die vier Elektronen im Überlappungsbereich gehören gleichzeitig zum linken UND zum rechten Sauerstoffatom. Dadurch kommen beide in ihrer 2. Schale auf insgesamt 8 Außenelektronen (Oktettregel). Und insgesamt hat dann jedes O-Atom 10 Elektronen (wie das Atom des Edelgases Neon; Edelgasregel).
Für (wesentlich) größere Moleküle oder solche mit vielen Bindungen wird das aber schnell unübersichtlich...
LG von der Waterkant
Für ein Molekül ergibt ein Schalenmodell nicht wirklich einen Sinn. In einfachen Fällen zeichnet man Lewisformeln, in die nur die Valenzelektronen eingehen, also die der äußersten Schale. Eine deutlich bessere Beschreibung liefert das Molekülorbital-Modell, das ist aber auch deutlich komplizierter. Über das PSE solltest du da schon deutlich hinaus sein.
“Für ein Molekül ergibt ein Schalenmodell nicht wirklich einen Sinn.“ das stimmt, aber vieles in der Schule ergibt keinen Sinn :D
Wir müssen es leider in der Klausur als Schalenmodell können, das habe ich mir nicht ausgedacht.
Trotzdem vielen Dank für die Antwort!🙌🏼
Aus dem PSE kannst du für Hauptgruppenelemente die Anzahl der "Schalen" und die Anzahl der Valenzelektronen direkt ablesen (Periode; Hauptgruppen-Nr. 1-8)
Eine sehr ausführliche und wirklich hilfreiche Antwort, danke!!