warum nehmen manche basen kein proton auf?
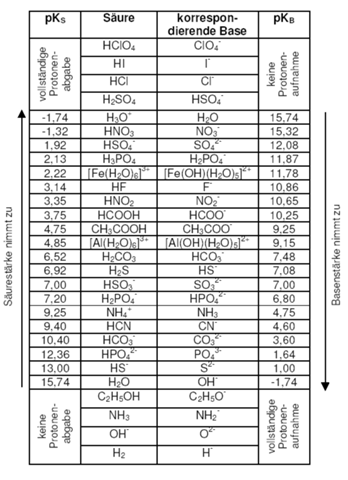
oben bei den korrespondierenden basen steht -keine protonenaufnahme-
warum? es ist ja eine base und basen nehmen normalerweise H+ auf
2 Antworten
Weil die korrespondierende Säure dermaßen stark ist, dass sie das Proton direkt abgibt. Denn je stärker eine Säure ist, desto schwächer ist ihre korrespondierende Base und umgekehrt.
(Randnotiz: Dass die genannten korrespondierenden Basen wie Cl^- keine Protonen aufnehmen, stimmt so eigentlich nicht. Auch die kann man dazu "zwingen". In einer stinknormalen wässrigen Lösung kann man allerdings guten Gewissens annehmen, dass kein Proton aufgenommen wird.)
Es gibt eine kristalline Verbindung (H3O) ClO4. In solchen Systemen nimmt also Wasser lieber ein Proton auf als Perchlorat.
Beachte, dass sich diese Tabelle auf wässrige Lösungen bezieht. Nur hier ist pH, pKs und pKb definiert. Diese Basen sind einfach zu schwach.