Chemie Säure Base pH-Wert Cyanidin?
Hi, kann mir jemand erklären, welcher pH-Wert welchem der jeweiligen Molekülstrukturen zugeordnet wird?
pH<3 heißt ja, dass eine starke Säure vorliegt ( Konzentration H3O+ überwiegt) ph= 8 leicht alkalisch also mehr OH^- Ionen
Aber beim Zuordnen und genaueren erklären, weiß ich nicht…
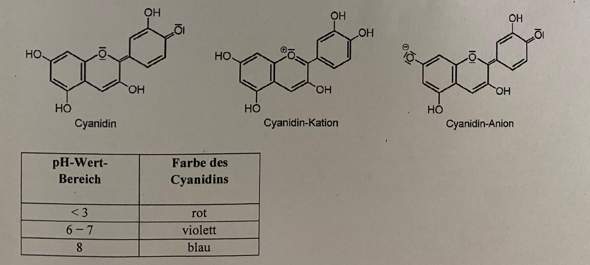
Also ich würde pH=8 beim Anion zuordnen, da hier eine negative Ladung herrscht, wodurch ein Proton leichter aufgenommen wird also alkalisch als base reagiert. Beim Kation pH<3, da ja eine positive Ladung herrscht und das Molekül ein Proton eher abgeben möchte, also als Säure reagiert und das Cyanidin an sich dann pH=6-7 .. leicht als säure?
2 Antworten
Deine Gedanken sind ja irgendwie ganz gut, aber du hast die Aufgabenstellung nicht verstanden. Cyanidin ist ein Indikator, der je nach pH-Wert eine andere Farbe zeigt. Die Aufgabe besteht nun darin, die gegebenen Strukturen des Cyanidins den Lösungen mit den gegebenen pH-Werten zuzuordnen.
In der sauren Lösung wird der Indikator also H+ aufgenommen und im Alkalischen abgegeben haben .
Damit ist es jetzt leicht!
danke dir! bei der aufgabe soll auch noch begründet werden im Zusammenhang mit dem chemischen Gleichgewicht… ?
Du musst den Farbstoff als Opfer und die Lösung als Täter betrachten. Ein Indikator wird ja nur in geringen Mengen zugegeben und andere Bestandteile der Lösung bestimmen deren pH-Wert.
Eine saure Lösung, also pH=3, führt dazu, dass der Indikator protoniert wird, also als Kation vorliegt. Eine basische Lösung, also pH=8, führt dazu, dass dem Indikator ein Proton entzogen wird, er also als Anion vorliegt.
Beim Kation musst du übrigens genau hinschauen, denn die positive Ladung ist beim O im mittleren Ring, das H am O.Atom im rechten Ring rechts. Es ist also eine Protonierung mit anschließender Ladungsverschiebung.
danke dir! bei der aufgabe soll auch noch begründet werden im Zusammenhang mit dem chemischen Gleichgewicht… ?
Säure-Basen-Gleichgewicht ist das Stichwort.
Henderson-Hasselbalch-Gleichung, wenn dir das was sagt.
Der niedrige pH-Wert beim Cyanidin Kation also hohe Konzentrstion an H3O+ Ionen führt dazu, dass das Cyanidin ein Proton aufnimmt und das Gleichgewicht sich auf die Seite der kationischen Form verschiebt. Beim hohen pHWert also Cyanidin lügen viele Hydroxidionen vor, daher gibt das Cyanidin ein Proton ab und das gleichgewicht verschiebt sich auf seite der Anionischen Form.. beim Cyanidin ist das gleichgewicht schon eingestellt ?
Der niedrige pH-Wert beim Cyanidin ...
Der pH-Wert gilt für die ganze Lösung, ist eine Eigenschaft der Lösung.
Ist wohl eher eine Formulierungsfrage, da solltest du mehr drauf achten. Es ist ein himmelweiter Unterschied, ob du "der pH-Wert beim Cyanidin führt ..." oder "der pH-Wert führt beim Cyanidin ..." schreibst.
stimmt denn meine zuordnung so? kation= ph<3 und anion pH=8 und normal 6-7?