Warum kann Hydrogencarbonat (HCO3) ein Ampholyt sein?
Frage steht in der Frage^^
3 Antworten

Ich möchte mal Picus Antwort für Dich etwas ausführlicher schreiben:
Betrachte Dir einmal das Hydrogencarbonatmolekül (1).
Dieses stammt von der Kohlensäure, die in wässriger Lösung ein Proton abgeben kann und somit zum einen ein Hydrogencarbonatanion und ein Oxoniumion hinterlässt (2).
Das Problem, welches Du bei der Kohlensäure hast, ist, dass diese keine besonders starke Säure ist, und daher nur sehr ungern ihr Proton abgibt und das Hydrogencarbonation daher wieder mit Wasser Kohlensäure und Hydroxid-Ionen bildet (2a) - auch diese Reaktion ist reversibel - man spricht dabei von einem chemischen Gleichgewicht.
Andererseits stellt das Hydrogencarbonatanion eine (schwache) Säure dar, die erneut ein Proton abgeben kann, worauf sich ein Oxoniumion und ein Carbonatanion in Lösung bildet (2b) - auch diese Reaktion ist reversibel und ein Gleichgewicht.
Die Eigenschaft, dass ein Säurerest entweder Protonen aufnehmen oder abgeben kann, wird als "ampholytisches Verhalten" in der Chemie bezeichnet.

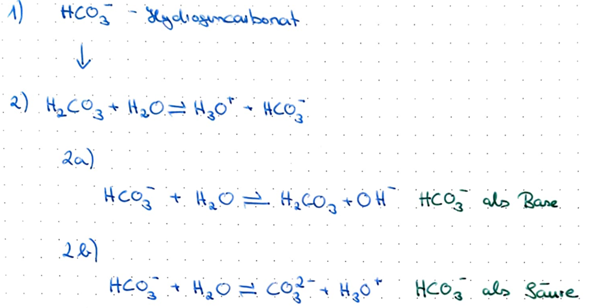

Weil es sowohl als Base, als auch als Säure reagieren kann.
Das Hydrogencarbonation (HCO3-) ist das Ion der Kohlensäure H2CO3 (schwache Säure), es kann mit Basen, wie z.B. CaOH2 zu (CO3)2- weiterreagieren
2HCO3- plus CaOH2 reagiert zu CaCO3 plus 2H2O
oder mit Säuren wie der Salzsäure wieder zur Kohlensäure
HCO3- plus HCl reagiert zu H2CO3 plus CL-
Darum ist das Hydrogencarbonat auch ein Puffer

Weil es ein Proton aufnehmen und auch ein Proton abgeben kann.
Ist das nicht ein bisschen kurz für eine Hausaufgabe? Kann man das noch länger und ausführlicher beschreiben?