Löslichkeitsprodukt, kann mir jemand erklären wie man auf die Lösung kommt?
Löslichkeitsprodukt, kann mir jemand erklären wie man auf die Lösung kommt?
2 Antworten

Das ganze danach natürlich noch mit multiplizieren, um diesen Prozentwert zu berücksichtigen.


Von gutefrage auf Grund seines Wissens auf einem Fachgebiet ausgezeichneter Nutzer
Chemie, Chemie, Naturwissenschaften
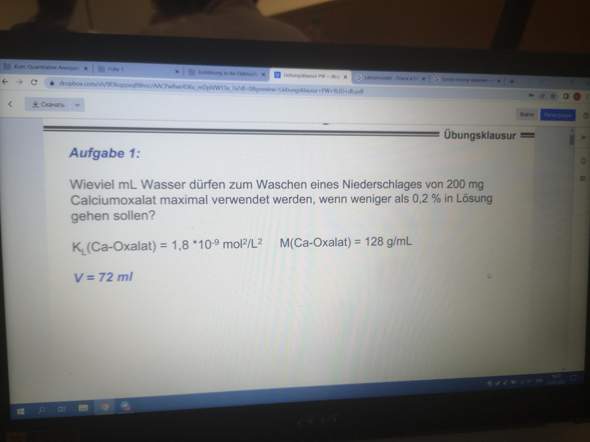
Wir haben das Löslichkeitsprodukt Kₛₚ=1.8⋅10⁻⁹ mol²/l² für die Reaktion
Ca²⁺ + C₂O₄²⁻ ⟶ CaC₂O₄↓
also beträgt die Löslichkeit von Calciumoxalat in reinem Wasser c=√Kₛₚ=4.2⋅10⁻⁵ mol/l bzw. als Massenkonzentration γ=cM=5.4 mg/l.
Du hast 200 mg Calciumoxalat und willst nicht mehr als 0.2% also m=0.4 mg davon verlieren, daher darfst Du mit maximal V=m/γ=74 ml Wasser waschen.
Woher ich das weiß:Studium / Ausbildung – Chemiestudium mit Diss über Quantenchemie und Thermodynamik