H-Atom an Radikal gezogen?
In der radikalischen Substitutionsreaktion wird im 1. Kettefortpflanzungsschritt das H-Atom zum Halogen Radikal gezogen.
Wieso ist das so? Und wie ist das mit dem Halogen Brom?
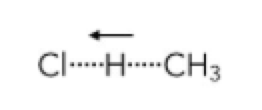
(Wasserstoffatom des Alkans zur rechten Seite wird vom Halogen Cl angezogen)
1 Antwort

Bei Chlor dürfte es ziemlich klar sein - die Elektronegativität von Chlor ist deutlich höher als die von Kohlenstoff, damit ist zu erwarten, dass Chlor auch Protonen (Wasserstoffionen) stärker binden kann.
Bei Brom ist es komplizierter - hier muss insgesamt sogar Energie aufgewendet werden, um ein H an das Br-Radikal zu übertragen. Immerhin passiert im Mikrokosmos so ziemlich alles, was irgendwie passieren kann, nur umso seltener, je mehr Energie (oder Vergleichbares) es kostet, und dann wird es auch schneller wieder rückgängig gemacht.
(Vgl. die Ergebnisse einer Websuche nach
radikalische substitution brom
vermutlich ist der Treffer
https://www.studysmarter.de/schule/chemie/organische-chemie/radikalische-substitution/
geeignet, um ein wenig mehr zu verstehen.)
Wenn ein genügend stabiles Endprodukt entsteht, hat man Glück - dann bleibt vom Endprodukt genug übrig.