Bewegung von Wasser bei der Osmose?
Hallo zusammen,
wir schreiben am Donnerstag eine Bioklausur, Hauptbestandteile werden die Zusammenarbeit von Zellorganellen und die Osmose sein.
Letztendlich ist die Osmose ja sehr logisch und verständlich: Alle Teilchen, sowohl in der Lösung, als auch im Lösemittel diffundieren ja ständig, nur die vom Lösungsmittel kommen aber durch die SEMIpermeable Membran.
Letzte Biostunde haben wir dann nochmal folgende Zeichnung erhalten:
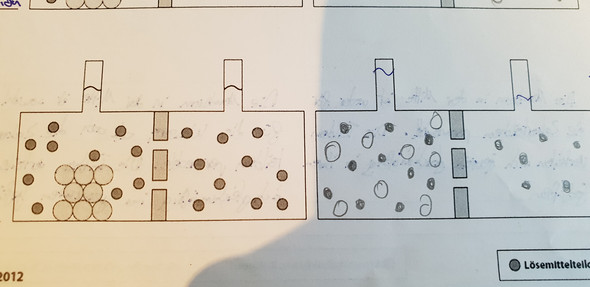
Wie man sehen kann, sind in der linken Abbildung von Anfang an auf beiden Seiten der Trennschicht gleich viele Lösemittelteilchen (was ich als AUSGANGSzustand schon fraglich finde). Dann, nach einiger Zeit bzw. im ENDzustand rechts, sind scheinbar links mehr Lösemittelteilchen als rechts - ich denke aber, da das Lösemittel ja diffundiert genau wie die Lösung, aber als einzige durch die Trennschicht kann, müssten doch erst jetzt, und nicht etwa im AUSGANGSzustand, auf beiden Seiten gleich viele Lösemittelteilchen sein und nicht auf der Seite mit der Lösung mehr als auf der anderen!
Oder gibt es da irgendeine "Kraft", die die Lösemittelteilchen, hier Wasser, tatsächlich in die Richtung der Lösungsteilchen "zieht"? Vielleicht haben wir die im Unterricht einfach nicht besprochen
Danke für die Antworten,
mfG Torge
4 Antworten

Stell dir mal vor, du hast dein Gefäß mit der Membran, wo nur das Lsgsmittel durchgeht. Darin ist zB Wasser, dann hast du von Anfang an gleich viele Wassermoleküle auf jeder Seite. Dann wirfst du einen Brocken Salz rein. Das ist das linke Bild, bevor er sich auflöst.
Im rechten Bild ist der Salzbrocken dann aufgelöst. Salz kann nicht durch die Membran, die Natur verlangt aber nach der möglichst gleichen Konzentration überall. Also wird Wasser rüberwandern und so werden mehr Wassermoleküle auf der salzigen Seite sein.

Du solltest solch eine Zeichnung nicht zu ernst nehmen.
Kannst du schon daran merken, dass im Steigrohr keine Teilchen sind. Was soll da also steigen?
Und selbstverständlich sind, wie du richtig erkannt hast, bei gleichem Wasserstand links weniger Lösungsmittelteilchen, ist schließlich weniger Platz, wegen des gelösten Stoffes.
Wenn durch Osmose Lösungsmittelteilchen nach links wandern, sind es dann irgendwann links gleich viele und irgendwann mehr als rechts. Allerdings nur dann, wenn auch Platz ist. Wenn da kein Steigrohr wäre, oder ein extrem dünnes, würde sich schon durch ganz kleine Mengen Lösungsmittel links ein enormer Druck aufbauen.
Der Druck ist es ja, der der Osmose Grenzen setzt.
Fazit: Ein gutgemeintes Bild, das einem oberflächlichen Menschen hilft, kann einen sehr genau hinsehenden Menschen durchaus in die Irre leiten.
Und nein, es gibt keine geheimnisvollen Kräfte. Eher zu viele oberflächliche Darstellungen, bildlich und schriftlich.
Wenn du die Klausur hinter dir hast, und Zeit und Interesse, die Osmose wirklich zu verstehen, dann schau dir die wissenschaftliche Arbeit an, die mich die Osmose hat verstehen lassen. Das erste und einzige mal, dass mir sowas passiert ist. Stammt von Einstein, aus dem Jahr 1905 meine ich.
Dort kannst du lernen, dass der osmotische Druck von den gelösten Teilchen ausgeübt wird, nicht vom Lösungsmittel. Als wäre das Lösungsmittel gar nicht da. Fand ich damals sehr spannend, und wurde v.a. vorher nie so erklärt. Also wo ich's vorher gelesen hatte, in Lehrbüchern, die nachher entstanden sind.
Und wenn's dir zu hoch ist, dann behalte es im Hinterkopf und sieh es dir in ein paar Jahren an.

Absoluter Scheiss heute da bereitet man sich so gut vor auf die Klausur und hat alles sowasvon gut verstanden und letztendlich sind es alles so fragen für die ich gar nicht hätte lernen KÖNNEN und in der Aufgabe wird danach verlangt alles genau zu beschreiben dann macht man das besser als vermutlich alle anderen in der Klasse hat aber keine Zeit mehr dann noch die nächste Teilaufgabe zu machen die man auch ez hinbekommen hätte

Die großen Kugeln (links noch im Verbund) gehen mit der Zeit in Lösung.
Wasser ist im Bestreben zum Konzentrationsausgleich nach links gewandert, da wurde ein Druck aufgebaut.

Schau dir die Osmose noch mal genau an, Wasser wandert durch die Membran.
Die Anzahl der gelösten Teilchen spielt eine Rolle.
Die Seite ist informativ:
http://daten.didaktikchemie.uni-bayreuth.de/umat/osmose/osmose.htm

Vielen Dank für die Seite, dort gibt es viele nützliche Informationen. Aber die Definition der Osmose bzw. die Versuchsbeobachtungen schließen doch immer noch auf die (teilweise) Falschheit der Zeichnung die ich geschickt habe: Auf Stoffebene sind zunächst in beiden Teilen des Behälters dieselben Volumen, auf Teilchenebene sind in dem mit der Salzlösung aber im Moment noch weniger Wassermoleküle als im Teil mit dem reinen Wasser. Was ich meine ist, dass in der linken Abbildung auf dem Zettel, den wir bekommen haben, links jedoch bereits jetzt ohne die Diffusion in beiden Teilen gleich viele Wassermoleküle sind und später in der rechten Abbildung nach der Diffusion im einen Teil mehr als im anderen.
Alle Definitionen etc. sagen jedoch eigentlich scheinbar aus, dass anfangs unterschiedliche Wasserkonzentrationen vorhanden sind bei gleichen Volumina und dann durch die Diffusion diese Konzentration auf beiden Seiten ausgeglichen wird (hier ist sie das jedoch nicht). Deshalb denke ich die Zeichnung die wir bekommen haben ist irreführend

Du hast Recht, die Abbildung ist blöd und falsch. Die Stoffmenge des Lösungsmittels muss in der linken Kammer kleiner sein.
Für das Lösungsmittel muss es ein Konzentrationsgefälle geben, dann strömt Wasser von der verdünnten zur konzentrierten Lösung.

Hey!
Ich habe das Thema auch gerade & ich glaube, dass du deine Antwort hier findest(irgendwo bei den aktiven Transportvorgängen):
https://www.frustfrei-lernen.de/biologie/biomembran-transportvorgaenge-diffusion-osmose.html
LG

Danke für den Link.. Ich glaube die letzten beiden Sätze vom Text zur Osmose haben meine Vermutung bestätigt. Und zwar sind, wie ich ja vermutet habe, zunächst in der Lösung weniger Wassermoleküle als im reinen Wasser (die Zeichnung die wir bekommen haben war also schonmal falsch), das ganze diffundiert dann und irgendwann ist die Konzentration des Wassers auf beiden Seiten ausgeglichen (hierzu bewegen sich ja Wassermoleküle von dem höher konzentrierten reinen Wasser zur weniger konzentrierten Salzlösung). Dadurch ist der Flüssigkeitsstand im Osmometer dann auf der Seite mit der Salzlösung höher als auf der mit dem reinen Wasser, obwohl auf beiden Seiten erst DANN dieselbe Anzahl an Wassermolekülen ist.
Hab ich glaub ich jetzt verstanden haha
Nochmal danke für den Link
mfG

Danke für die gute Zusammenfassung, so kann ich es bei mir jetzt auch aufschreiben haha
LG

Gerne aber verlass dich nicht zu 100% drauf haha :D aber so wie ich es geschrieben habe macht es am meisten Sinn denk ich
Genau, aber es müssten doch nach der Diffusion (rechte Zeichnung) in beiden Seiten des Behälters gleichviele Wassermoleküle sein und nicht im linken mehr als im rechten (dafür würde ja Energie notwendig sein und es wäre kein passives Verhalten mehr was gegen die Definition der Osmose ginge) oder nicht