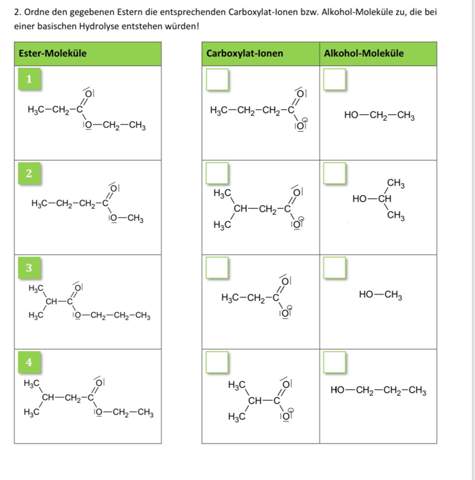
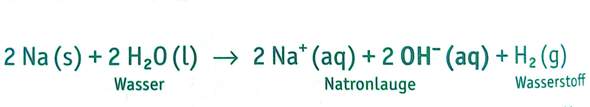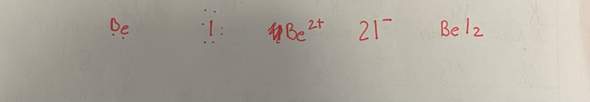die molare Löslichkeit von Mn(OH)2 in einer 0,020 mol/L NaOH LSG in sauren Lösung (PH2) und in einer basischen Lösung (PH12) soll berechnet werden. KLP= 1,6 * 10^-5 (Löslichkeitsprodukt). Wie mach ich so eine Aufgabe?
Verwandte Themen
Chemie frage?
Labor,
Base,
Biochemie,
Chemieunterricht,
Chemikant,
Ionen,
mol,
Säure,
Neutralisation,
ph-Wert,
chemische Reaktion,
molare Masse,
Reaktionsgleichung,
Säuren und Basen,
Stöchiometrie,
Titration