Wie genau sind Metalle untereinander angeordnet?
Ich habe vorhin eine Antwort auf eine Frage gesehen, wo es darum ging, wie Metall-Kationen untereinander eine Bindung eingehen können. Klar, nicht die Kationen der Metalle sondern die Metalle selbst gehen Bindungen untereinander ein... aber wie genau? Ich weiß dass diese eine Elektronenwolke um die Rümpfe haben aber wie kann ich mir das genau vorstellen?Was genau bedeutet hier Rumpf? Atom etwa? Und diese E-Wolke, ist das das Band wovon immer die Rede ist? Ich würde das Prinzip dahinter gerne verstehen,
danke :)
2 Antworten
Elektronenband besteht aus Elektronen gespaltener Energieniveaus.
Bei gebundenen Metallatomen spalten sich die diskreten Energieniveaus auf.
Sie liegen nah beieinander und bilden ein breiteren Energiebereich(Energieband).
Die Energieniveaugruppen bilden Energiebänder mit verbotenen Zonen dazwischen.
Die Energiebänder sind bei zunehmenden Abstand vom Atomkern breiter.
Bei kleinerem Atomabstand werden die Abstände der gespaltenen Energieniveaus größer.
Ab einem höheren Atomabstand überschneiden sich die Energiebänder und werden zum durchgehenden Leitungsband.
Die Elektronen im Leitungsband sind nicht an Atome gebunden und können sich frei im Metallgitter bewegen (Leitfähigkeit von Elektrizität und Wärme).
Die äußeren Elektronen sind also nicht so stark an den Atomkern gebunden.
Atomrumpf ist der Atomkern mit den inneren Elektronen ohne die Außenelektronen im Valenzband und Leitungsband.
Bei Metallbindungen sind die Abstände zwischen den Atomkernen im Allgemeinen kleiner als bei ionischen und kovalenten Bindungen, die Atome sind dichter.
Die Atomrümpfe sind in einem Metallgitter angeordnet, die Struktur hängt vom Metall ab.
Elektronenwolke ist die räumliche Verteilung von Elektronen um Atomkern oder Molekül und umfasst auch die inneren Elektronen.
Das was du meinst nennt sich Elektronengaswolke.
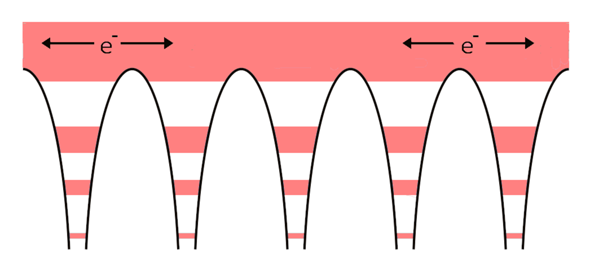
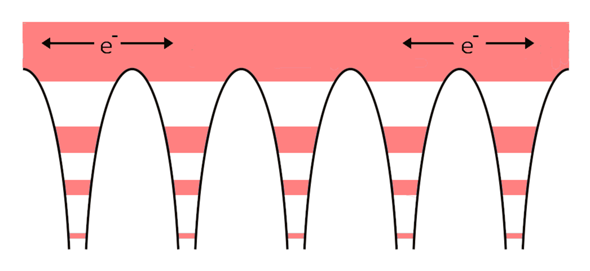
Hier ist das Prinzip der metallischen Bindung beschrieben.