Warum ist die Elektronegativität von Argon so gering?
Hallo,kann mir jemand sagen ,warum hat Argon so eine niedrige Elektronegativität hat?
Es ist ja eigentlich ein Edelgas und müsste somit ja auch auf die letzte ,,Schale” eine hohe Anziehungskraft ausüben.Also müsste es ,wenn ihm ein Elektron fehlt,andere Elektronen sehr stark anziehen,oder liege ich da falsch?
5 Antworten

Hallo!
Offensichtlich haben Edelgase kein Elektronegativität, weil seine Elektronenhüllen aus Valenzelektronen gefüllt sind, so dass sie nur an sehr wenigen chemischen Reaktionen teilnehmen können: es sind nur wenige hundert chemische Verbindungen der Edelgasen bekannt.
P.S. Argos (aus griechischen) - langsam
Mit freundlichen Grüßen :)

Vom Argon existiert m.W. nur eine Verbindung HArF. Vielleicht reicht das nicht, eine EN zu bestimmen, vielleicht hat sich keiner die Mühe gemacht oder vielleicht ist sie in die meisten EN-Tabellen noch nicht eingearbeitet.
Die Pauling-Skala auf wikipedia nennt 2,6 für Xe (vergleichbar mit Kohlenstoff) und 3,0 für Kr (vergleichbar mit Stickstoff). Da die EN in der 3. Periode nur wenig höher ist als in der 4. Periode, könnte man für Kr irgendwas um 3,2 erwarten, so zwischen Stickstoff und Sauerstoff.
Deine letzte Überlegung kann ich nicht so ganz teilen. Zwar zieht Ar "seine" Elektronepaare stark an, aber Atome kennen kein Eigentum. Bindende Elektronenpaare werden von beiden Atomen als "ihre" betrachtet, die brauchen nicht allein ihre zu sein.

Rein von der Logik/Theorie her, hätte Argon eigentlich einen sehr hohen EN-Wert. Als Element der 8. HG würde es einen Teufel tun seine stabile Konfiguration loszuwerden.
Eher würde es um so stärker Elektronen anziehen. DIe Tendezen im PSE sind, dass der En Wert von oben nach unten abnimmt und von links nach rechts zunimmt ;)
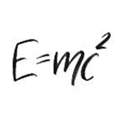
Argon kann keine Bindungen eingehen, er haht gar keine Elektronegativität.
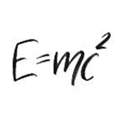
Seine Valenzschale ist mit 8 Elektronen besetzt. Er ist von Natur aus im Edelzustand

Edelgase besitzen keine Elektronegativität, weil die Elektronegativität ein Maß dafür ist, wie sehr z.B. ein Ar Atom in einer Bindung Elektronen zu sich selbst herzieht. Edelgase gehen aber keine Bindungen ein und gönnen sich einfach das ganze Elektron im Fall der Fälle.

Es gibt zig oder hunderte Edelgasverbindungen, die meisten vom Xenon.