Vorgehensweise beim Aufstellen von Valenzstrichformeln/LEWIS-Formeln?
Guten Tag,
ich habe Probleme beim Aufstellen von Strukturformeln mir unbekannter Moleküle, daher möchte ich wissen, wie ihr vorgeht bzw. ob es irgendeine Art Schema/Regel gibt, die ich befolgen kann. zB. für HNO3, S2O3 2-
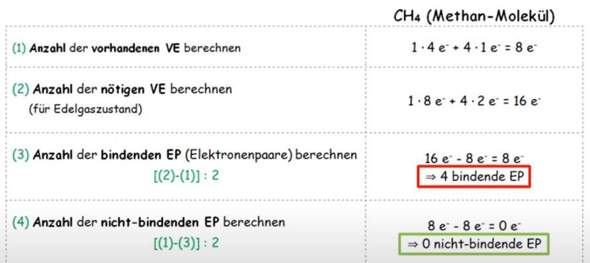
Ich habe bereits eine Vorgehensweise im Internet gefunden, welche im angehängten Bild zu sehen ist, jedoch lässt sich diese nicht wirklich auf negativ/positiv geladene Moleküle übertragen und dauert auch etwas.
3 Antworten
Bei Ionen musst du die Anzahl der Elektronen reduzieren/erhöhen, je nach Ladung.
- notiere die Atome der Verbindung
- Zeichne nach Lewis die Valenzelektronen zu jedem Atom (als Punkte)
- überlege dir, wie die Atome verbunden sind
- verbinde die Elektronen (Punkte) entsprechend.
- Wenn es Ionen sind: Überlege dir, wo und was da wohl gebunden war (meist H). Wenn es negativ geladen ist, dann bleibt ein bindendes Elektronenpaar zurück, wenn es positiv ist, dann fehlt ein Elektron.
- Zeichne das Molekül bzw. Molekülion schöner...
Zum Üben nimm Beispiele, deren Struktur du kennst und zeichne es nach dem Schema.
Da gibts kein einheitliches Schema für, das immer funktioniert. Das liegt einfach daran, dass es ganz oft (besonders für größere Moleküle) nicht nur eine Möglichkeit gibt, die Atome zusammenzubauen.