Verdünnung von Säuren?
Moinsen, und zwar habe ich eine kurze Frage, da ich grade auf Wikipedia folgenden Satz unter den Eigenschaften von Säuren gefunden habe: Säuren kann man mit Wasser verdünnen, dabei wird ihre Wirkung je nach Verdünnung deutlich schwächer. Das Verdünnen von konzentrierten Säuren ist eine exotherme Reaktion. Es entsteht also Wärme. Vor allem beim Verdünnen von konzentrierter Schwefelsäure kann die Säurelösung unkontrolliert wegspritzen. Daher gilt beim Verdünnen die Regel, die Säure in das Wasser zu geben, nicht umgekehrt.
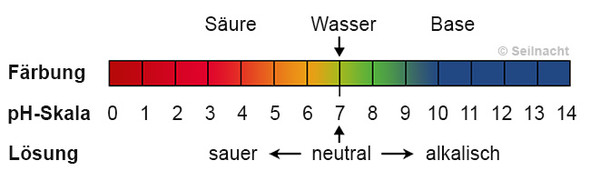
Meine Frage wäre: um was für einen pH-wert wird die Säure ungefähr schwächer? Die pH-wert Skala geht ja von 0-14, und beispielsweise die Säure hat einen Wert von 4 und wird mit Wasser verdünnt. Wird der wert ca. 3 oder 2 sein?
Vielen dank für eine eventuelle Hilfe!MfG l1nk17
5 Antworten
Daher gilt beim Verdünnen die Regel, die Säure in das Wasser zu geben, nicht umgekehrt
das wäre von Vorteil !
Wenn man säure verdünnt wird sie weniger sauer. Also wenn dei ausgangswert ph 4 wäre, würde die verdünnte säure einen entsprechend höheren ph wert haben. Wie weit der ph wert steigt, hängt davon ab wieviel wasser du nimmst...
Also wenn du die Säure verdünnst bekommt sie einen pH-Wert über 4 und nicht da unter, da sie ja nicht saurer wird. Wie hoch der pH-Wert geht hängt natürlich davon ab, mit wie viel Wasser du verdünnst.
Das kannst du so nicht beantworten. Dazu muss u.A. folgendes bekannt sein:
- Welche Säure?
- Konzentration unverdünnte Säure
- Konzentration verdünnte Säure
Du weißt aber schon, dass 3 oder 2 saurer ist als 4?
Es kommt aber eben darauf an, wie die Verdünnung ist. Sagen wir du hast HCl mit der Anfangskonzentration 1 mol/l. Da wirst du rechnerisch einen pH von 0 haben. Willst du jetzt 10 fach verdünnen oder 100 fach oder ganz anders? Bei 0,1 M HCl hättest du pH = -log0,1. Bei starken Säuren kannst du ja quasi davon ausgehen, dass sie vollständig dissoziieren.
mein versehen, lese ich grade erst! ja, weiß ich.