Thermische Zersetzung, Druck aus enthalpie und Entropie berechnen?
Was habe ich bei der c) falsch gemacht? Sollten der Sauerstoffzersetzungsdruck bei zunehmender Temperaturen nicht zunehmen?

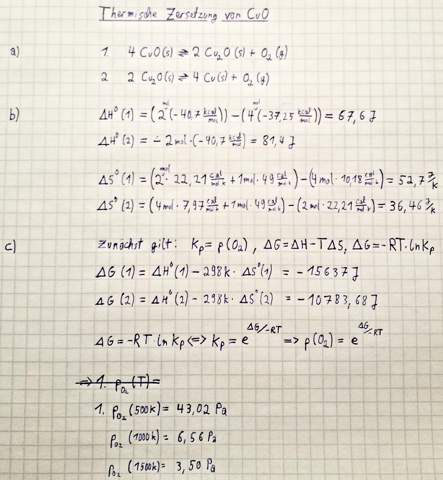
1 Antwort

Von gutefrage auf Grund seines Wissens auf einem Fachgebiet ausgezeichneter Nutzer
chemische Reaktion, Reaktionsgleichung, Chemie
Schon die Reaktionsenthalpie ist falsch, dann kann der Rest auch nicht stimmen. Dass die freie Reaktionsenthalpie nicht stimmen kann, müsste dir selbst auffallen, das Gleichgewicht würde ja völlig auf der Produktseite liegen.
Woher ich das weiß:Berufserfahrung

Muss ich beispielsweise zum Schluss bei p(T) auch die Temperatur von ∆G variieren oder nur das 1/(-RT)?

@ADFischer
Ist das bei Differenzen nicht absolut egal? Eine änderung um x cal ist das gleiche wie eine änderung um x J.

Stimmt, ich bin hier von umgekehrten edukten und Produkten ausgegangen, danke. Ist denn abgesehen von dem Folgefehler das Vorgehen soweit richtig?