Temperaturberechnung innerhalb der Gibbs-Helmholtz-Gleichung?
Wenn ich die Reaktionsenthalpie und die Reaktionsentropie habe. Und die Aufgabe wäre das ich die Temperatur T berechnen soll ab der eine Reaktion freiwillig abläuft.
Wie müsste ich dort vorgehen? Vielleicht nach T umstellen?
2 Antworten
Du musst für DeltaG den Wert "0" einsetzen. Dann ist alles gegeben, um T auszurechnen.
Wichtig: Du hast jetzt die Grenztemperatur für "freiwillig <=> unfreiwillig" ausgerechnet. In der Antwort musst du aber angeben, ob die Reaktion oberhalb oder unterhalb dieser Grenztemperatur freiwillig abläuft.
Das kannst du durch überlegen herausfinden oder, indem du einfach einen anderen Wert für T einsetzt: Wenn DeltaG negativ wird, befindest du dich auf der richtigen Seite der Grenztemperatur.
Alles klar?
Natürlich, was sonst.
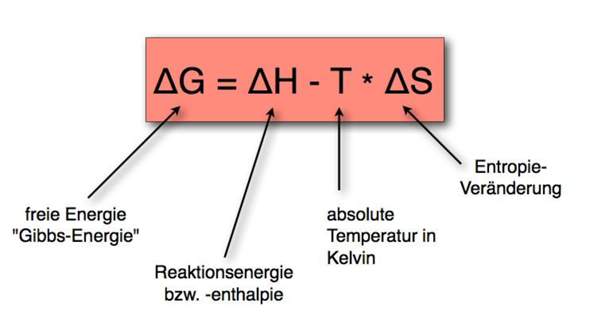
(Übrigens wundert mich, dass das Gibbs-Potential hier als "freie Energie" bezeichnet wird - vgl. die Tabelle bei https://de.wikipedia.org/wiki/Thermodynamisches_Potential#Beschreibung und https://www.abiweb.de/chemie-antrieb-und-steuerung-chemischer-reaktionen/chemische-thermodynamik-energetik/zustandsgroessen-und-ihre-regeln/freie-enthalpie.html)