Reaktionsgeschwindigkeit Chemie?
hallo zusammen,
ich bin in meiner Vorbereitung auf meine kommende Chemie Arbeit auf folgende Aufgabe gestoßen zur Reaktionsgeschwindigkeit. Wie komme ich beim berechnen auf folgende Werte? (Erstes Bild ist die Aufgabe zweites Bild die Lösung)
Danke im Voraus🥰

Aufgabe 3c)

1 Antwort

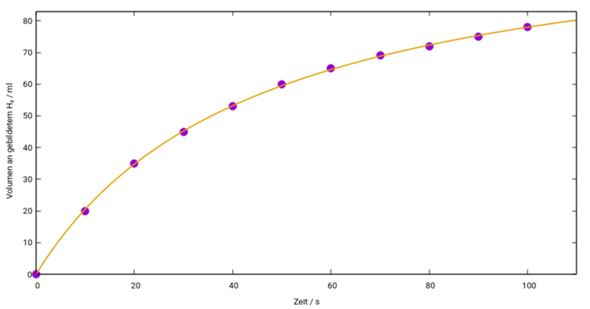
Hier ist das graphisch aufgetragen, mit einer Ausgleichskurve der Form k₁t/(1+k₂t), mit k₁=2.51028±0.02651 ml/s und k₂=0.0221997±0.0003942 s⁻¹. Man sieht, daß die Reaktionsgeschwindigkeit abnimmt, vermutlich, weil immer mehr Mg-Oberfläche verschwindet und die Reaktion nur an der Metalloberfläche abläuft.
Die erste Ableitung davon ist, wenn ich einem online-Rechner trauen kann, k₁/(k₂t+1)². Sinnigerweise rechnet man die momentanen Reaktionsgeschwindigkeiten zu einem Zeitpunkt t über diese Ableitung aus, z.B. nach 10 s 1.68 ml/s oder nach 20 s 1.20 ml/s.