Hilfe Chemie SOS?
Hi, ich schreibe am Montag einen Test in Chemie und ich verstehe das Thema Chemisches Rechnen leider überhaupt nicht! Ich mach gerade eine Übungsaufgabe die lautet:
Bei der quantitativen Elementaranalyse von 0,1000 g einer farblosen organischen Flüssigkeit wurden 0,1882 g Kohlenstoffdioxid und 0,1188 g Wasser gebildet. Die Molmasse der Substanz wurde zu 46 g bestimmt.
Welche Summenformel hat die Verbindung?
Bis jetzt habe ich das erarbeitet:
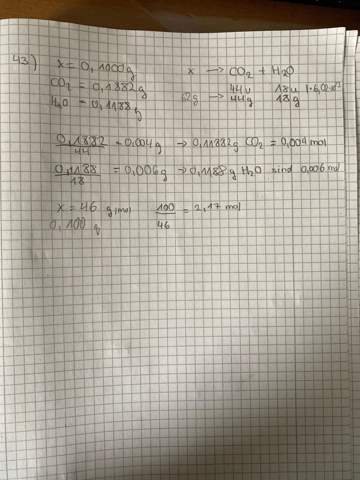
Bei den letzten beiden Zeilen habe ich keine Ahnung was ich da gemacht habe. Ich verstehe leider überhaupt nicht wie ich auf die Lösung kommen soll, kann mir bitte bitte irgendwer helfen oder erklären was ich jetzt machen soll?
Tausend dank!
2 Antworten
Folgende Punkte sind wichtig:
- Welche Elemente sind in der Flüssigkeit enthalten? Gesättigt?
- Reaktionsgleichung!
- Stoffmengenkonstanz: Mole von C und H bleiben gleich, O kommt dazu
- Achtung: molekulare Gase?
Das meiste hast du gut angefangen, nur in der Mitte werde ich nicht schlau. Die Einheiten und Rundung sind falsch.
Ich kann dir schon einmal sagen, dass Gesamtmasse = 0,3070 g und somit 0,2070 g O dazugekommen.
Die Kohlenstoffzahl ist wichtig: Teile dafür n(CO2)/n(Stoff).
Den Wasserstoff bestimmst du durch 2*n(H2O)/n(Stoff).
Der Sauerstoff ist etwas tricky und nicht immer dabei. Gucke dazu, wie viel Massendifferenz noch fehlt oder wie viel O2 hinzugekommen ist, damit die Gleichung stimmt. Hier hilft zur Not ausprobieren.
Ich hoffe, dass ich weiterhelfen konnte. Fragen in die Kommentare.
Ja mit einer einfachen und bekannten Molmasse ist es leicht. Aber eine Systematik hat das nicht!
1. Rechne mit Einheiten.
2. Rechne mindestens mit 3 signifikanten Ziffern.
3. Verwende Formeln und Formelzeichen!
Der Anfang ist richtig, aber falsch und unvollständig notiert. Und ohne die Formeln geht der Weg schnell verloren, außerdem ist es ungenau (nur 1 Stelle)!
n(CO2)=m(CO2)/M(CO2)=0,1882 g/44 u=0,00428 mol = 4,28 mmol
n(H2O)=m(H2O)/M(H2O)=0,1188 g/18 u=0,00660 mol => 13,2 mmol =n(H)
m(O)=m0-m(C)-m(H)=m0-n(CO2)×M(C)-2×n(H2O)×M(H)
m(O)=0,100 g -0,00428 mol×12 u-2×0,0066 mol×1 u= 0,035 g
n(O)=m(O)/M(O)=0,035 g/16 u=0,0022 mol = 2,2 mmol
C:H:O=4,3 : 13,2 : 2,2 | ÷2,2 = 1,95 : 6 : 1 = 2:6:1
=> C2nH6nOn
Da M=46 u passt nur n=1, also C2H6O.
Es ginge Ethanol (wahrscheinlich, flüssig) und Dimethylether (unwahrscheinlich, gasförmig)
Vielen Vielen Dank! Das ist super. Aber wie bist du in der 6. Zeile auf 13,2 mmol gekommen?