Chemie: welche Verbindung am schlechtesten wasserlöslich?
Kann mir bitte jemand erklären woran man das festmacht?
1 Antwort
Von gutefrage auf Grund seines Wissens auf einem Fachgebiet ausgezeichneter Nutzer
Wasser, Alkane, Chemieunterricht
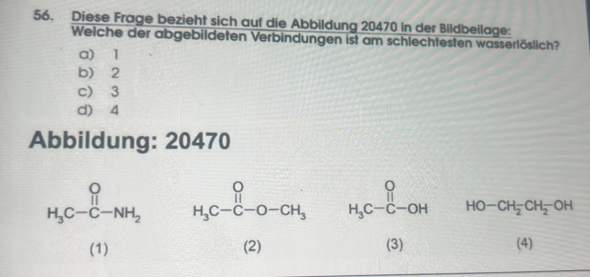
- Acetamid CH₃CONH₂ ist sehr gut wasserlöslich, weil die Amidgruppe sehr polar ist; in einem Liter Wasser lösen sich grob 2 kg Acetamid.
- Ameisensäuremethylester CH₃COOCH₃ ist passabel wasserlöslich (ca. 300 g/l), weil die Estergruppe moderat polar ist und die kurzen Alkylreste daran nichts ändern.
- Essigsäure CH₃COOH ist wegen der COOH-Gruppe sehr polar und unbeschränkt mit Wasser mischbar.
- Glycol CH₂OH–CH₂OH hat zwei OH-Gruppen und ist deshalb superpolar und fähig, viele H-Brücken auszubilden; es mischt sich unbeschränkt mit Wasser.