(Anti-)auxochrome Gruppen von DCPIP/Tillmanns Reagenz?
Hey, kann mir evtl jemand die auxochromen und antiauxochromen Gruppen der folgenden drei Teilchen markieren. Bitte mit Unterscheidung welche Gruppe antiauxochrom und welche auxochrom ist. (Gerne auch Erklärung was genau die speziell an dem Teilchen so machen). Vielen Danke! :)
(Muss morgen meine Seminararbeit präsentieren und habe Angst vor den äußert spezifischen Fragen für die meine Lehrkraft bekannt ist)
P.S. das erste Teilchen ist farblos, das zweite tiefblau und das dritte rosa, falls es weiterhilft. Die Farbigkeit grob erklärt habe ich schon, bräuchte wirklich nur die Gruppen, danke :)
1 Antwort

Hi,
die Unterscheidung in auxochrom und antiauxochrom ist davon abhängig, ob die Substituenten einen +M-Effekt oder einen -M-Effekt auf das Chromophor (das zugrunde liegende Doppelbindungssystem) ausüben.
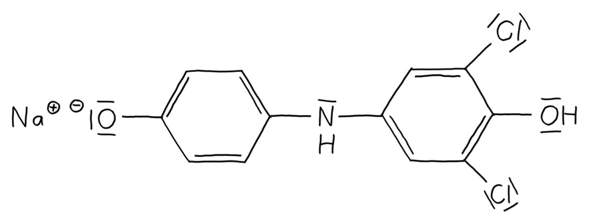
Molekül AEs liegen vor: Ein deprotonierter Sauerstoff mit einem Natrium-Gegenion, zwei Chlorsubstituenten und eine Hydroxygruppe.
- O-: Hat drei freie Elektronenpaare. Übt also einen +M-Effekt auf das Chromophor aus, ist auxochrom.
- Cl, OH: Auch diese Substituenten üben einen +M-Effekt aus, sind auxochrom.
Wir haben also insgesamt vier Substituenten mit einem +M-Effekt auf zwei Seiten des Moleküls. Das ist eher ungünstig, weil wir so nur relativ wenig Mesomerie im System haben (die Elektronenpaare können nicht gut "klappen"). Durch die vergleichsweise geringe Mesomerie liegt das Absorptionsmaximum des Moleküls im nicht sichtbaren Bereich. Das Molekül erscheint farblos.
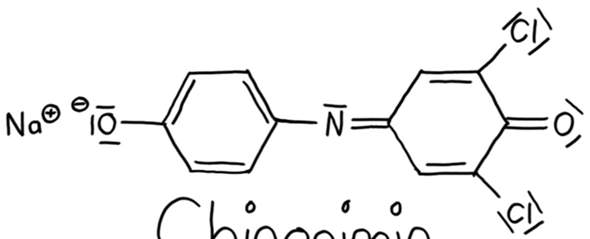
Molekül BEs liegen vor: Ein deprotonierter Sauerstoff mit einem Natrium-Gegenion, zwei Chlorsubstituenten und Sauerstoffsubstituent.
- O-: Hat drei freie Elektronenpaare. Übt also einen +M-Effekt auf das Chromophor aus, ist auxochrom.
- Cl: Auch diese Substituenten üben einen +M-Effekt aus, sind axcochrom.
- O: Dieser Substituent übt einen -M-Effekt aus, ist antiauxochrom.
Wir haben also drei Substituenten mit einem +M-Effekt und einen mit einem -M-Effekt. Das ist günstiger als im ersten Molekül, weil wir durch einen "push-and-pull-Effekt" nun mehr Mesomerie im System haben (die Elektronenpaare können über das gesamte Molekül vom O zum O- "klappen"). Durch die höhere Mesomerie liegt das Absorptionsmaximum des Moleküls im sichtbaren Bereich. Das Molekül erscheint blau.
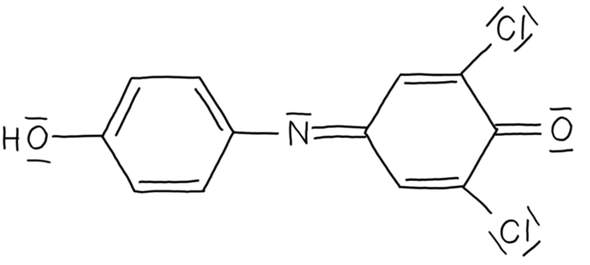
Molekül CEs liegen vor: Ein protonierter Sauerstoff(also OH), zwei Chlorsubstituenten und ein Sauerstoffsubstituent.
- OH: Hat zwei freie Elektronenpaare. Übt also einen +M-Effekt auf das Chromophor aus. Jedoch einen schwächeren als O-, ist auxochrom.
- Cl: Auch diese Substituenten üben einen +M-Effekt aus, sind auxochrom.
- O: Dieser Substituent übt einen -M-Effekt aus, ist antiauxochrom.
Wir haben also wieder drei Substituenten mit einem +M-Effekt und einen mit einem -M-Effekt. Der -M-Effekt bei OH ist aber schwächer als beim deprotonierten Sauerstoff O-, die wahrgenommene Farbe ist also schwach rot.
LG