anode kathode oxi red?
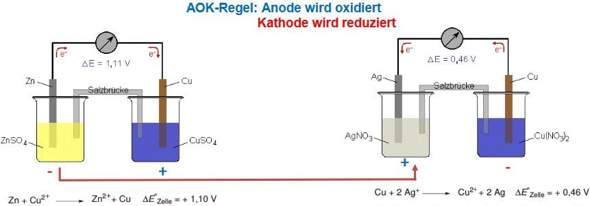
kann mir jemand erklären warum hier die Anode oxidiert wird und die Kathode reduziert?
1 Antwort

Von gutefrage auf Grund seines Wissens auf einem Fachgebiet ausgezeichneter Nutzer
Chemie
Die Anode ist immer die Elektrode, an der die Oxidation stattfindet. Oder meinst du, welche der beiden Elektroden jeweils die Anode ist? Das siehst du am Normalpotential. Das Metall mit dem niedrigeren Normalpotential wird jeweils oxidiert. Bei der Kombination Cu/Zn ist das Zink, bei Ag/Cu ist Kupfer das weniger edle Metall und wird oxidiert.
Woher ich das weiß:Berufserfahrung

@ADFischer
Die Linke znso4 Lösung ist minus warum? Da wird doch Zink oxidiert, die Lösung sollte positiv sein.
Beim Plus pol fliesen Elektronen hin, da wird doch reduziert? Auf der linken Seite Fliesen die Elektronen zu Kupfer, dann findet dort die Reduktion statt?