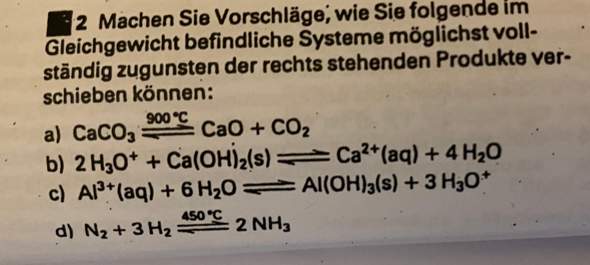
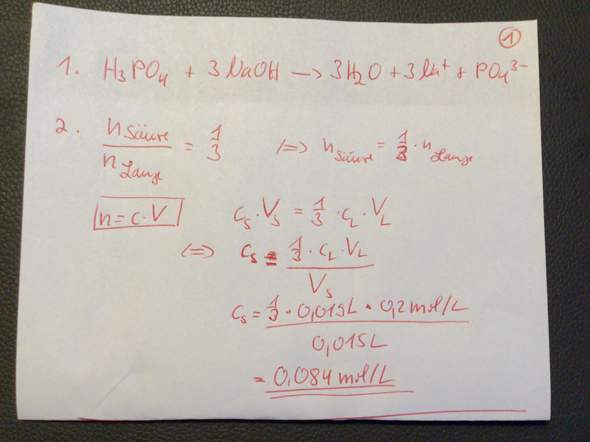Wenn man in ein nach oben geöffnetes Gefäß Wasser und gasförmiges CO2 hinzufügt und das Gefäß mit einer Kolbe schließt , und demnächst die Kolbe nach unten drückt, dann wird der Druck erhöht.
Deshalb reagieren feste CO2 erstmal zu flüssigem CO2 im Wasser, das wiederum mit Wasser zu HCO3-(aq) reagiert. (CO2(aq)+2 H2O(l) ⇄H3O+(aq) + HCO3-(aq))
Liegt es daran, dass CO2(aq) weniger Volumen als CO2(g) hat und bei geringerem Volumen CO2(g) eher günstiger ist? Oder liegt es nur daran, dass bei der zweiten Reaktion die Anzahl der Moleküle von 3 auf 2 verringert wird?(Und deshalb mehr Volumen gesichert ist?)
Vielen Dank.