Hallo,
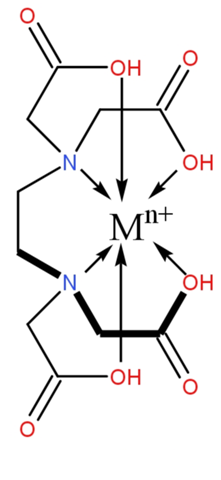
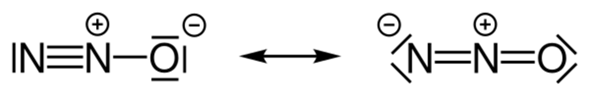
ich verstehe nicht wie die Hybridisierung der Atomorbitale bei N und O (vielleicht auch F?) funktioniert, bzw. was der Sinn dabei ist?
Dass C oder B dadurch ein freies Valenzelektron mehr bekommt und dadurch auch mehr Bindungen eingehen können, leuchtet mir ein. Wie das bei N oder O aber aussehen soll, verstehe ich nicht. Sie haben ja schon jedes p-Orbital mindestens einmal besetzt und bekommen durch die Hybridisierung ja keines mehr hinzu. Höchstens würden sie ja das doppelt besetzte s-Orbital durch ein doppelt-besetztes p-Orbital ersetzen...
Auch frage ich mich wie das bei sp, sp2 und sp3-Hybridisierungen dann abläuft. Ich gehe mal davon aus, dass zuerst das px-Orbital gesenkt wird, dann das py und zu guter Letzt das pz-Orbital bin mir aber nicht sicher darüber...
Danke.