Wie bekommt man Diabetes?
4 Antworten
Hallo 46gtu58bh95, 👋
Wie bekommt man Diabetes?
"Diabetes“ ist nur ein Überbegriff für mehrere,
verschiedene (12) Diabetes-Erkrankungen,
bzw. Diabetes-Typen.
Die häufigsten sind Typ1-, und Typ2- Diabetes.
~~~~~~~
Typ1-Diabetes ist eine Autoimmunerkrankung
und hat mit der Ernährung, dem Gewicht
und der Bewegung überhaupt nichts zu tun.
An Typ1-Diabetes erkranken idR normalgewichtige,
schlanke, oder dünne Menschen, die sich
gesund ernährt haben, sportlich sind,
bzw. sich ausreichend bewegt haben.
An Typ1-Diabetes kann JEDER Mensch in
JEDEM Alter erkranken. An Typ1-Diabetes
erkranken mehr Erwachsene (4150),
als Kinder und Jugendliche (3100).
Die Ursachen werden noch erforscht.
~~~~~~~~~~~~~~~~~~~~~~~~~~~~~~~
Typ2-Diabetes ( = Übergewichts-Diabetes)
ist eine Stoffwechselerkrankung und
entsteht hauptsächlich
DURCH starkes Übergewicht/Adipositas
UND jahrelange oder jahrzehntelange
schlechte, ungesunde Ernährung
UND chronischen Bewegungsmangel.
Meistens ist auch eine genetische Disposition
(familiäre Vorbelastung) vorhanden.
~~~~~~~
LG 🙋🏻♀️🪶
Bist du bei Google gebannt?
Neben einer erblichen Veranlagung gelten Übergewicht und Bewegungsmangel als die wichtigsten Verursacher eines Typ-2-Diabetes. Aber auch eine unausgewogene (ballaststoffarme, fett- und zuckerreiche) Ernährung und Rauchen begünstigen die Entstehung von Typ-2-Diabetes.
https://www.diabinfo.de/leben/typ-2-diabetes/grundlagen/ursachen-und-entstehung.html
sei froh das du das nicht hast
Erst einmal: Zucker kann kein Typ 2 Diabetes verursachen. Das ist biochemisch nicht möglich. Die wissenschaftlich kausale Ursache ist Fett, egal woher es kommt: Nahrungsfette, vom Körperfett produzierte Fette, vom Zucker umgewandelte Fette. Diese Fette führen zur mitochondrialen Dysfunktion, Insulinresistenz, Lipotoxizität, Hyperinsulinämie, Hyperglykämie, gesteigerten Fettproduktion und Glukoseproduktion in der Leber.
Wie Typ 2 Diabetes wirklich entstehtInsulinresistenz: Seit 1927 ist wissenschaftlich bekannt, dass Nahrungsfette eine Insulinresistenz verursachen. Circa 70 Jahre später, als man z.B. mit der ¹H-NMR-Spektroskopie in die Zellen schauen konnte, um zu gucken was da eigentlich passiert, war auch der Mechanismus bekannt:
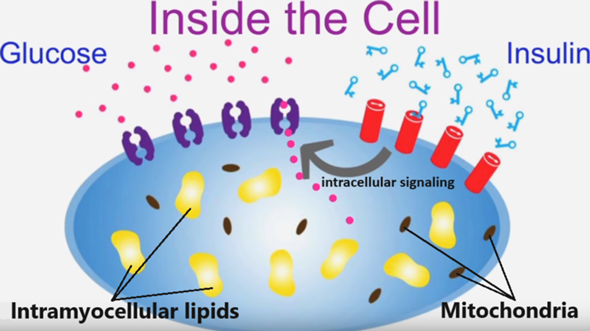
Bei fettreichen Mahlzeiten gelangen, anstelle der Glukosemoleküle, die Fettsäuren in die Muskel- und Leberzellen – intra(myo)zelluläre Lipide – und produzieren freie Radikale und toxische Abbauprodukte (Lipidmetabolite) wie Diacylglycerine und Ceramide, die das Funktionieren der Insulin-Signalwege erschweren, indem die inneren Insulinrezeptoren blockiert und die Enzyme der Insulinrezeptoren, die eigentlich die GLUT4 Glukosetransporter aktivieren sollen, gehemmt werden. Das von der Bauchspeicheldrüse produzierte Insulin bindet dann zwar an den Insulinrezeptoren außerhalb der Zellen, aber im Inneren der Zellen passiert nichts. Die Folge: Insulin wird wirkungslos, als Ausgleich wird mehr Insulin benötigt und produziert (Hyperinsulinämie), und Glukose sammelt sich im Blut an (Hyperglykämie).


Warum werden Zucker und Übergewicht mit Diabetes in Verbindung gebracht?
Wenn man eine Menge Bauchfett hat, ist dieses Bauchfett metabolisch aktiv und produziert entzündungsfördernde Zytokine (Interleukin-1, Interleukin-6), die zusätzlich die Insulinrezeptoren außerhalb der Zellen stören, und Fettsäuren, die Insulinresistenz fördern.
Zucker wird bei gesunden Menschen nicht in Fett umgewandelt, sondern erst, wenn man im Kalorienüberschuss ist, wenn man isolierte Fruktose (z.B. hunderte Gramm Fruchtzuckerpulver) zu sich nimmt, oder wenn die Fettproduktion (De-novo-Lipogenese) in der Leber durch Insulinresistenz oder Fettleber gesteigert ist. Dieses Fett fördert Insulinresistenz.
Insulin Deficiency and Insulin Inefficiency
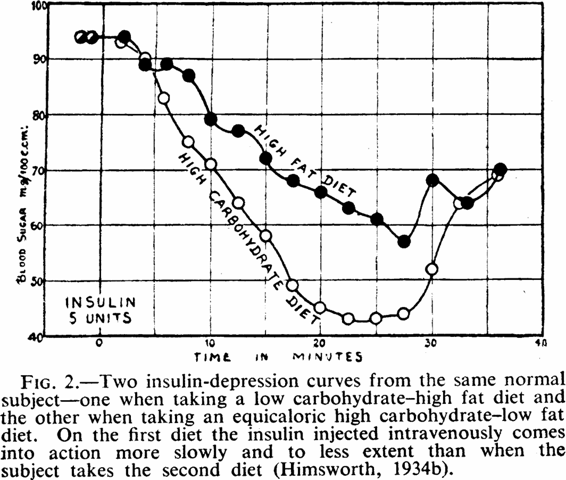
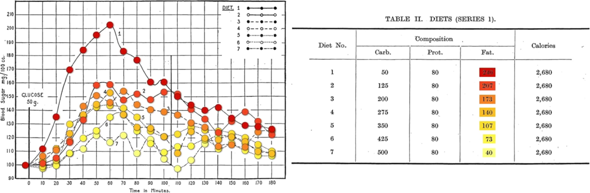
1940: Erstmals 1927 fand man heraus, dass das Fett in der Ernährung die Glukosetoleranz beeiträchtigt, weswegen der Blutzuckerspiegel nach fettreichen Mahlzeiten stärker ansteigt und langsamer sinkt.

Abbildung 1: Zwei Blutzucker-Toleranzkurven desselben Probanden: Bei der kohlenhydratarmen, fettreichen Diät ist die Glukosetoleranz beeinträchtigt, bei der kohlenhydratreichen, fettarmen Diät ist sie verbessert.

Abbildung 2: Zwei Insulin-Depressionskurven desselben Probanden: Bei der kohlenhydratarmen, fettreichen Diät wirkt das intravenös gespritzte Insulin langsamer und in geringerem Maße als bei der kohlenhydratreichen, fettarmen Diät.
DIETARY FACTORS THAT INFLUENCE THE DEXTROSE TOLERANCE TEST
1927: Bei der Gruppe mit der fettreichen Ernährung schoss die Glukoseintoleranz in die Höhe. Bei gleicher Zuckerwassermenge reagierte sie mit einem doppelt so hohen Blutzuckerspiegel.
Relationship of dietary saturated fatty acids and body habitus to serum insulin concentrations: the Normative Aging Study
1993: Würde der Anteil der gesättigten Fettsäuren an der Gesamtenergie von 14% auf 8% sinken, so würde das Nüchterninsulin nach einer Mahlzeit um 18% und das postprandiale Insulin um 25% abnehmen. Sowohl Körperfett als auch der Verzehr von gesättigten Fettsäuren können einen Insulinüberschuss im Blut verursachen. Wenn wir den Konsum gesättigter Fettsäuren reduzieren, können wir diesen Prozess unterbrechen. Eine Verringerung der Aufnahme von gesättigten Fettsäuren hat erhebliche Auswirkungen auf den Insulinspiegel und die Senkung des Bedarfs an überschüssigem Insulin, unabhängig davon, wie viel Bauchfett wir haben.
Mechanism of free fatty acid-induced insulin resistance in humans
1996: Es wurde festgestellt, dass eine erhöhte Konzentration freier Fettsäuren im Plasma eine Insulinresistenz durch Hemmung des Glukosetransports verursacht.
Intramyocellular lipid concentrations are correlated with insulin sensitivity in humans: a 1H NMR spectroscopy study
1999: Bei gesunden Jugendlichen geht eine akute Erhöhung der freien Fettsäuren im Plasma (durch eine Intralipid-Infusion) mit einem signifikanten Anstieg der intramyozellulären Lipide und einer Verringerung der Insulinsensitivität einher, unabhängig von der ethnischen Zugehörigkeit.
Rapid impairment of skeletal muscle glucose transport/phosphorylation by free fatty acids in humans
1999: Nach nur 3 Stunden kann es passieren, dass Fett eine Insulinresistenz verursacht, indem die Glukoseaufnahme gehemmt wird.
Overnight lowering of free fatty acids with Acipimox improves insulin resistance and glucose tolerance in obese diabetic and nondiabetic subjects
1999: Reduziert man den Fettgehalt im Blut, verringert sich die Insulinresistenz und der Blutzucker.
Plasma fatty acid composition and incidence of diabetes in middle-aged adults: the Atherosclerosis Risk in Communities (ARIC) Study
2003: Nach Anpassung für Alter, Geschlecht, BMI, Verhältnis von Taille zu Hüfte, Alkoholkonsum, Zigarettenrauchen, körperliche Aktivität, Bildung, Vorgeschichte von Diabetes in der Familie, war die Diabetesinzidenz signifikant und positiv mit den Anteilen der Cholesterinester und der Fettsäuren der Phospholipide im Plasma verbunden.
Impaired mitochondrial activity in the insulin-resistant offspring of patients with type 2 diabetes
2004: Die Insulinresistenz im Skelettmuskel ist mit einer Dysregulation des intramyozellulären Fettsäurestoffwechsels verbunden. Dieser Anstieg des intramyozellulären Lipidgehalts war höchstwahrscheinlich auf eine mitochondriale Dysfunktion zurückzuführen.
Mechanisms underlying skeletal muscle insulin resistance induced by fatty acids: importance of the mitochondrial function
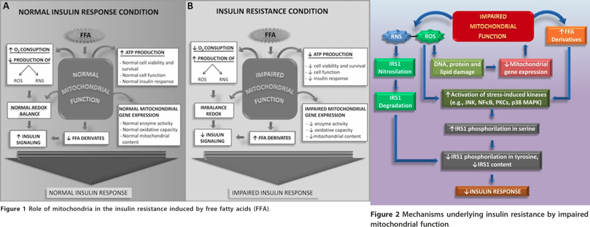
2012: Ein erhöhter Gehalt an freien Fettsäuren im Plasma spielt eine wichtige Rolle bei der Entwicklung einer Insulinresistenz der Skelettmuskulatur. Eine Insulinresistenz wird mit der Entwicklung verschiedener Syndrome wie Fettleibigkeit, Typ-2-Diabetes und metabolisches Syndrom in Verbindung gebracht. Für die durch Fettsäuren induzierte Insulinresistenz der Muskeln wurden mehrere Mechanismen postuliert, darunter der Randle-Zyklus, oxidativer Stress, Entzündungen und mitochondriale Dysfunktion.

Abbildung 1: Die Rolle der Mitochondrien bei der durch freie Fettsäuren induzierten Insulinresistenz: Im Normalzustand verstoffwechseln Mitochondrien freie Fettsäuren effizient und mit geringer Produktion reaktiver Sauerstoffspezies (ROS), wodurch die Insulinreaktion erhalten bleibt. Im pathologischen Zustand führen hohe Plasmaspiegel freier Fettsäuren zu einer erhöhten Aufnahme in die Zellen und Mitochondrien. Dies beeinträchtigt die mitochondriale Biogenese und Funktion, reduziert die oxidative Kapazität und führt zur Anhäufung von Lipidmetaboliten sowie einer gesteigerten ROS- und reaktiven Stickstoffspezies (RNS)-Produktion. Die Folge ist die Aktivierung von Proteinkinasen, die die Insulin-Signalübertragung durch fehlerhafte Phosphorylierung und Nitrosilierung des Insulinrezeptorsubstrats-1 (IRS-1) stören, was letztlich die Insulinantwort beeinträchtigt.
Effects of an overnight intravenous lipid infusion on intramyocellular lipid content and insulin sensitivity in African-American versus Caucasian adolescents
2013: Gibt man Fett in den Blutkreislauf von Jugendlichen, sammelt es sich in ihren Muskelzellen an und reduziert ihre Insulinsensitivität. Hohe Blutfettwerte spielen eine wichtige Rolle bei der Insulinresistenz, sowohl bei gesunden als auch bei übergewichtigen Menschen, mit oder ohne Typ 2 Diabetes.
Dietary fat acutely increases glucose concentrations and insulin requirements in patients with type 1 diabetes: implications for carbohydrate-based bolus dose calculation and intensive diabetes management
2013: Nahrungsfette erhöhen akut die Glukosekonzentration im Blut und den Insulinbedarf.
Skeletal intramyocellular lipid metabolism and insulin resistance
2015: Die in Skelettmuskelzellen gespeicherten Lipide werden als intramyozelluläre Lipide bezeichnet. Störungen im Zusammenhang mit den intramyozellulären Lipiden und ihrem ursächlichen Faktor, den zirkulierenden freien Fettsäuren im Blutkreislauf, führen zu einem toxischen Zustand und letztlich zu einer Insulinresistenz im Muskelgewebe.
https://www.youtube.com/watch?v=3igKW6bl3FE
Schon nach wenigen Stunden einer fettreichen Mahlzeit entwickelt sich eine kurzzeitige Insulinresistenz. Die isolierten Fettsäuren aus den Ölen kommen am schnellsten ins Blut. Eine chronisch hohe Fettaufnahme kann zu einer dauerhaften Insulinresistenz führen, wenn der Fettstoffwechsel ständig gestört ist, und man verliert die Fähigkeit, Kohlenhydrate richtig zu verstoffwechseln.
LipotoxizitätDie Lipotoxizität ist ein Zustand, der durch die schädliche Wirkung von überschüssigen Fettsäuren auf Gewebe und Organe verursacht wird, insbesondere bei Menschen mit Diabetes oder Insulinresistenz. Sie tritt auf, wenn der Körper zu viele freie Fettsäuren produziert oder nicht richtig verarbeiten kann, was zu einer Ansammlung von Fetten in nicht dafür vorgesehenen Geweben führt, wie etwa der Leber, der Bauchspeicheldrüse, den Muskeln und dem Herzen, und sie trägt zur Verschlimmerung der Stoffwechselstörungen bei Diabetes bei und ist mit verschiedenen negativen Auswirkungen verbunden:
- Erhöhte Insulinresistenz: Fettansammlungen in der Leber und den Muskeln stören den Glukosestoffwechsel und erhöhen die Insulinresistenz.
- Schädigung der Betazellen: In der Bauchspeicheldrüse führen Fettsäuren zu einem Verlust der Insulinproduktion.
- Entzündungen: Die Fettablagerungen und die toxischen Derivate führen zu Entzündungsreaktionen, die die Gewebe weiter schädigen.
- Herz-Kreislauf-Erkrankungen: Die Lipotoxizität kann auch die Funktion des Herzens und der Blutgefäße beeinträchtigen und das Risiko für Herz-Kreislauf-Erkrankungen erhöhen.
Fatty acids and glucolipotoxicity in the pathogenesis of Type 2 diabetes
2008: Obduktionsstudien zeigen, dass die Zahl der Betazellen bei der Diagnose von Typ-2-Diabetes bei etwa 50% liegt und nach vielen Jahren auf etwa 20% abnimmt. Die Endozytose von LDL-Cholesterin kann durch die Bildung von ROS (freien Radikalen) zum Absterben der Betazellen führen. In ähnlicher Weise beeinträchtigte eine anhaltende Erhöhung der zirkulierenden nicht-veresterten freien Fettsäuren durch Lipidinfusion die Funktion der insulinproduzierenden Betazellen, insbesondere bei Personen mit einer genetischen Veranlagung. Eine westliche Ernährung, reich an gesättigten Fetten, führt zu Fettleibigkeit, Insulinresistenz und erhöht die Konzentration der freien Fettsäuren.
The long lifespan and low turnover of human islet beta cells estimated by mathematical modelling of lipofuscin accumulation
2009: Nach ungefähr 20 Jahren haben wir bereits alle insulin-produzierenden Betazellen in unserer Bauchspeicheldrüse. Es werden keine neuen produziert.
mTOR: from growth signal integration to cancer, diabetes and ageing
2010: Tierische Proteine sind übermäßig mit der Aminosäure Leucin angereichert, die das mTOR Enzym überstimuliert und zum Absterben der Betazellen führt. Pflanzen haben von Natur aus wenig Leucin.
Death protein 5 and p53-upregulated modulator of apoptosis mediate the endoplasmic reticulum stress-mitochondrial dialog triggering lipotoxic rodent and human β-cell apoptosis
2012: Gesättigte Fettsäuren steigern das Betazell-abtötende Death Protein 5 (DP5). Gesättigte Fettsäuren schaden den Betazellen, sodass diese nicht mehr angemessen auf die Kohlenhydrate, die wir zu uns nehmen, reagieren können.
Lipotoxicity: effects of dietary saturated and transfatty acids
2013: Gesättigte Fettsäuren steigern lipotoxische freie Fettsäuren, die toxisch auf unsere Betazellen wirken. Fettsäurederivate können die Funktion der Betazellen beeinträchtigen und letztlich zu ihrem Tod durch Lipoapoptose führen.
Saturated free fatty acid sodium palmitate-induced lipoapoptosis by targeting glycogen synthase kinase-3β activation in human liver cells
2013: Gesättigte Fettsäuren wie Natriumpalmitat, die vor allem in Fleisch und Milchprodukten enthalten sind, sind fast durchgängig toxisch in Zellkulturen, während die einfach ungesättigten Fettsäuren wie Oleat, die in Oliven, Nüssen oder Avocados enthalten sind, entweder nicht toxisch oder sogar zytoprotektiv sind. Die durch die gesättigte Fettsäure Natriumpalmitat induzierte Lipoapoptose in menschlichen L02- und HepG2-Zellen wird durch eine GSK-3β-Aktivierung reguliert, die zur JNK-Aktivierung und Bax-Hochregulierung führt.
Low Protein Intake Is Associated with a Major Reduction in IGF-1, Cancer, and Overall Mortality in the 65 and Younger but Not Older Population
2014: Eine hohe Proteineinnahme steigert die Sterblichkeit um 75%, die Wahrscheinlichkeit an Krebs zu sterben um 300%, die Wahrscheinlichkeit an Diabetes zu sterben um 400%. Ursache ist der Anstieg von IGF-1 durch tierische Proteine.

Je mehr Fett, trotz weniger Kohlenhydrate, desto höher der Blutzucker.
Die effektivste BehandlungHigh-carbohydrate, high-fiber diets for insulin-treated men with diabetes mellitus
1979: Diabetiker bekamen eine fettarme, kohlenhydratreiche, ballaststoffreiche Ernährung mit über 300 Gramm Kohlenhydraten und 18 Gramm Fett (9% ihrer Kalorien) am Tag: Die tägliche Insulindosis wurde bei jedem der 20 Patienten niedriger. Die Insulintherapie konnte bei 11 Patienten abgesetzt werden, wovon 9 Patienten vorher 15-20 Einheiten/Tag und 2 Patienten 32 Einheiten/Tag hatten. Die Nüchternblutzuckerspiegel und 3-stündigen postprandialen Blutzuckerspiegel waren bei den meisten Patienten niedriger, trotz niedrigerer Insulindosen. Die Serumcholesterinwerte sanken von 206 mg/dl auf 147 mg/dl.
Veganism and its relationship with insulin resistance and intramycellular lipid
2004: 24 Veganer gegen 25 Omnivore (gleiches Geschlecht, Alter, Taillenumfang, BMI, Körperfett, Aktivitätslevel, Kalorienanzahl): Veganer aßen 10% mehr Kohlenhydrate, hatten trotzdem niedrigere Nüchternblutzuckerspiegel, 30% signifikant weniger intramyozelluläre Lipide, niedrigeren systolischen Blutdruck. Ihre Ernährung schützte die Betazellen der Bauchspeicheldrüse und das Herz-Kreislauf-System.
A Low-Fat Vegan Diet Improves Glycemic Control and Cardiovascular Risk Factors in a Randomized Clinical Trial in Individuals With Type 2 Diabetes
2006: Die Verbesserungen der Blutzucker- und Lipidkontrolle bei Typ-2-Diabetikern waren bei einer fettarmen, kohlenhydratreichen, veganen Ernährung größer als bei einer Ernährung, die auf den Richtlinien der American Diabetes Association (Diabeteswissenschaftler) orientiert.
A low-fat vegan diet and a conventional diabetes diet in the treatment of type 2 diabetes: a randomized, controlled, 74-wk clinical trial
2009: Die Veganer hatten 31% weniger intramyozelluläre Lipide als die Nicht-Veganer, die einer klassischen Ernährung gegen Diabetes folgten.

Die wissenschaftlich kausale Ursache ist Fett
FALSCH !
Du hattest Deine fehlerhaften Behauptungen bereits mehrfach als falsch bestätigt. Warum also nun wieder die gleichen falschen Behauptungen...?
.
Diabetes mellitus Typ 1 und Typ 2
Diabetes mellitus (Zuckerkrankheit) ist ein Überbegriff für verschiedene Erkrankungen des Stoffwechsels. Allen gemeinsam ist, dass sie zu erhöhten Blutzuckerwerten führen, weil die Patientinnen und Patienten einen Mangel am Hormon Insulin haben und/oder die Insulinwirkung vermindert ist.
Medizinisch unterscheidet man verschiedene Diabetes-Formen. Die Hauptformen sind der Typ-1- und der Typ-2-Diabetes mellitus. In Deutschland ist bei etwa 10 Prozent der Erwachsenen ein ärztlich diagnostizierter Diabetes mellitus bekannt. Über 90 Prozent davon sind an Typ-2-Diabetes erkrankt. Aufklärung und Vorbeugung sind die entscheidenden Stellschrauben zur Bekämpfung von Diabetes.
Typ-2-Diabetes
- entsteht zum einen durch eine verminderte Empfindlichkeit der Körperzellen für Insulin (Insulinresistenz), zum anderen führt eine jahrelange Überproduktion von Insulin zu einer "Erschöpfung" der insulinproduzierenden Zellen (die Bauchspeicheldrüse kann nicht genügend Insulin für den erhöhten Bedarf liefern),
- beginnt meist schleichend,
- wurde früher auch als "Altersdiabetes" bezeichnet, jedoch erkranken in den letzten Jahren auch zunehmend junge Erwachsene, sogar Jugendliche daran.
- Neben einer erblichen Veranlagung gelten Übergewicht und Bewegungsmangel als die wichtigsten Verursacher eines Typ-2-Diabetes. Aber auch eine unausgewogene (ballaststoffarme, fett- und zuckerreiche) Ernährung und Rauchen begünstigen die Entstehung von Typ-2-Diabetes.
- Es stehen verschiedene Therapiebausteine zur Verfügung. Am wichtigsten sind zunächst regelmäßige Bewegung, angepasste Ernährung und ein normales Körpergewicht. Dies verbessert die Empfindlichkeit der Körperzellen für Insulin und kann so den Insulinbedarf senken. Zu Beginn der Therapie wird deshalb immer versucht, mit Allgemeinmaßnahmen, wie konsequente Lebensstiländerungen, auszukommen.
- Sind Allgemeinmaßnahmen nicht erfolgreich, stehen verschiedene Medikamente zur Verfügung, die zum Beispiel als Tabletten eingenommen werden können. Erst wenn es auch mit diesen Medikamenten nicht gelingt, die Erkrankung in den Griff zu bekommen, muss auch bei Typ-2-Diabetes Insulin gespritzt werden.
Quelle: Bundesministerium für Gesundheit
.
Bitte mal Begründungen und Beweise für deine Aussagen vorlegen.
Soviel Aufwand für so wenig Fakten. Eine Ansammlung von Falschaussagen und völlig falschen Schlussfolgerungen.
Und täglich neu, mit neuem Account.
(1/4) Effect of non-oil-seed pulses on glycaemic control: a systematic review and meta-analysis of randomised controlled experimental trials in people with and without diabetes
2009: Gekochte Bohnen sind ähnlich effektiv bei der Hemmung der a-Glucosidase (Verlangsamung der Zuckeraufnahme) wie das beliebte Antidiabetikum Acarbose.
Regression of Diabetic Neuropathy with Total Vegetarian (Vegan) Diet
2009: Bei einer fettarmen, ballaststoffreichen, rein pflanzlichen Ernährung erfuhren 17 der 21 Patienten mit Typ 2 Diabetes und systemischer distaler Polyneuropathie in nur 4 bis 16 Tagen eine vollständige Linderung der scharfen, brennenden Schmerzen. Das Taubheitsgefühl blieb bestehen, verbesserte sich aber deutlich. Je länger sich die Patienten am Plan hielten, desto mehr verbesserte sich die Linderung. Am 14. Tag waren die Nüchternblutzuckerspiegel bei den 11 Patienten um 35% gesunken. Der Insulinbedarf hatte sich bei der Hälfte der Patienten verringert. Fünf von ihnen benötigten keine blutzuckersenkenden Mittel mehr. Gewichtsabnahme, Serumtriglyceride und Gesamtcholesterin verbesserten sich.
Vegetarian diets and incidence of diabetes in the Adventist Health Study-2
2011: Je weniger Tierprodukte, desto geringer die Häufigkeit für Typ 2 Diabetes.
Higher insulin sensitivity in vegans is not associated with higher mitochondrial density
2013: Veganer haben eine bessere Insulinsensitivität, weniger intrazelluläre Lipide, niedrigere Nüchternblutzuckerspiegel, niedrigere Insulinspiegel und bessere Glukoseaufnahme in den Zellen.
Effect of rice diet on diabetes mellitus associated with vascular disease
2016: Erstmals in den 50ern wurde in der "Rice Diet" Studie gezeigt, dass eine rein pflanzliche, kohlenhydratreiche Ernährung die diabetische Retinopathie zurückbilden kann. 30% der Patienten, die vorher z.B. keine Überschriften lesen konnten, entwickelten wieder eine normale Sicht. Im Vergleich kann unsere moderne Medizin nur das Fortschreiten der Erkrankung verlangsamen, z.B. mit Medikamenten oder einer Laser-Therapie.
Reversal of Pulmonary Hypertension, Diabetes, and Retinopathy after Adoption of a Whole Food Plant-Based Diet
2019: Case Study: Eine Person wurde von Typ 2 Diabetes, diabetische Retinopathie und pulmonale Hypertonie mit einer pflanzlichen Whole Food Ernährung geheilt, was die Medikamente vorher nicht geschafft haben.
Short-Chain Fatty Acids and Their Association with Signalling Pathways in Inflammation, Glucose and Lipid Metabolism
2020: Ballaststoffe aus der Nahrung werden von Darmbakterien im Dickdarm zu kurzkettigen Fettsäuren (SCFAs) umgewandelt und sind damit der wichtigste Faktor in der Ernährung um GLP-1 zu steigern. SCFAs können die Sekretion vom GLP-1 stimulieren, indem sie FFAR2 aktivieren, das indirekt den Blutzuckerspiegel reguliert, indem es die Insulinsekretion erhöht und die Glucagonsekretion der Bauchspeicheldrüse verringert. (Ballaststoffe sind somit effektiver als Ozempic.)
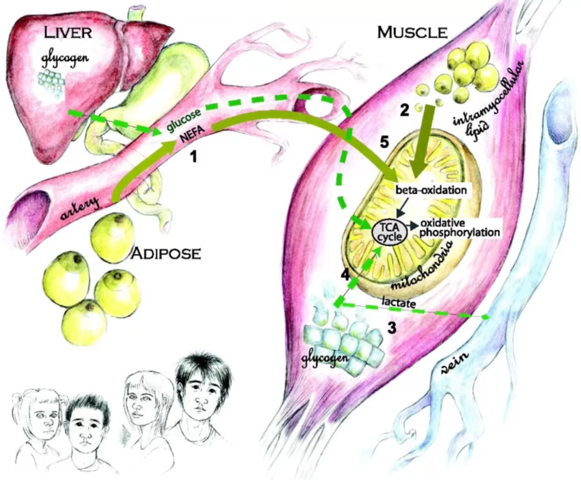
Pathogenese des metabolischen Syndroms: Die Bedeutung der ektopen Fettablagerung in Leber und Skelettmuskulatur
2005: Fett verursacht Metabolisches Syndrom. Abbildung 1: Durch die mitochondriale Dysfunktion in der Skelettmuskulatur von Nachkommen von Typ-2-Diabetikern ist die Fettsäuren-Oxidationskapazität eingeschränkt. Vermehrt anfallende Fettsäuremetaboliten führen zum Auftreten der Insulinresistenz und einer in der Folge verminderten Glukoseaufnahme (1). Auch aus dem Fettgewebe freigesetzte Fettsäuren und Zytokine begünstigen die Insulinresistenz der Skelettmuskulatur (2). Kompensatorisch kommt es zu einer vermehrten Insulinausschüttung aus den β-Zellen des Pankreas (3). Die Hyperinsulinämie fördert jedoch in der Leber die De-novo-Lipogenese, obwohl die Glukoseproduktion der Leber selbst durch die erhöhten Insulinspiegel nicht mehr unterdrückt werden kann («gemischte hepatische Insulinresistenz» [4]). Auch vermehrt aus dem Fettgewebe freigesetzte Fettsäuren und Zytokine fördern die Entstehung einer Fettleber und die hepatische Insulinresistenz (5). Schließlich werden auch die pankreatischen β-Zellen durch die erhöhten zirkulierenden Fettsäuren geschädigt («Lipotoxizität» [6]), und bei nachlassender Insulinsekretion kommt es zum Auftreten eines manifesten Diabetes.
Typ 1 Diabetes Behandlung
Auch Typ 1 Diabetiker entwickeln eine Insulinresistenz, wenn sie sich fettreich ernähren, deswegen sollten sie sich fettarm, kohlenhydratreich, ballaststoffreich ernähren, um weniger Insulin spritzen zu müssen.
Low Carb beseitigt zwar die Symptome, verstärkt aber die Insulinresistenz. Die Ketonkörper bei einer ketogenen Ernährung können zwar die intramyozellulären Lipide aus den Zellen bekommen – die Insulinresistenz lässt sich also zurückbilden – führen aber zu Nierenerkrankungen und Osteoporose. Beide Ernährungsformen fördern außerdem Cholesterinspiegel, Herz-Kreislauf-Erkrankungen, Krebs, Retinopathie und andere Krankheiten, und sind daher nicht zu empfehlen.
Video: Warum man Typ 2 Diabetes auf keinen Fall mit LowCarb oder Keto behandeln sollte
(2/4) Eine Fettleber steht im engen Zusammenhang mit einer Insulinresistenz. Die Ursachen für Lebererkrankungen wie Fettleber sind Cholesterin und gesättigte Fettsäuren, nicht Zucker.
Nonalcoholic fatty liver disease
2002: Abbildung 2 Panel B: Die aus der Insulinresistenz resultierende Hyperinsulinämie erhöht die Fettsäuresynthese (De-novo-Lipogenese) in den Hepatozyten durch Steigerung der Glykolyse und begünstigt die Anhäufung von Triglyceriden in den Hepatozyten durch Verringerung der hepatischen Produktion von Apolipoprotein B-100.
Dietary habits and their relations to insulin resistance and postprandial lipemia in nonalcoholic steatohepatitis
2003: Die Nahrungsaufnahme der 25 Patienten mit nicht-alkoholischer Steatohepatitis (NASH) enthielt mehr gesättigte Fettsäuren und Cholesterin, weniger mehrfach ungesättigte Fettsäuren, Ballaststoffe und antioxidative Vitamine C und E. Der Insulinempfindlichkeitsindex war bei NASH-Patienten signifikant niedriger als bei den Kontrollpersonen. Die Triglyzeridwerte waren bei NASH-Patienten höher als bei den Kontrollpersonen. Die Aufnahme gesättigter Fettsäuren korrelierte mit dem Insulinempfindlichkeitsindex, mit den verschiedenen Merkmalen des metabolischen Syndroms und mit dem postprandialen Anstieg der Triglyceride. Die postprandiale Reaktion auf Apolipoprotein B-48 und Apolipoprotein B-100 war bei NASH-Patienten flach und deutlich von der Triglyceridreaktion abgekoppelt, was auf einen Defekt der ApoB-Sekretion schließen lässt. Ernährungsgewohnheiten können die Steatohepatitis direkt durch die Modulation der hepatischen Triglyceridakkumulation und der antioxidativen Aktivität sowie indirekt durch die Beeinflussung der Insulinempfindlichkeit und des postprandialen Triglyceridstoffwechsels fördern.
Pathogenesis of type 2 diabetes: tracing the reverse route from cure to cause
2008: Die Insulinresistenz begünstigt die Entwicklung einer Fettleber bei einem Kalorienüberschuss. Ist die Insulinresistenz erst einmal etabliert, wird die erhöhte Insulinsekretion - die zur Aufrechterhaltung des Plasmaglukosespiegels erforderlich ist - die Fettablagerung in der Leber weiter verstärken. Die Fettleber führt zu einer Resistenz gegen die Unterdrückung der hepatischen Glukoseproduktion durch Insulin sowie zu einem erhöhten Triacylglycerinspiegel im Plasma. Wenn die Betazellen erhöhten Mengen an Fettsäuren ausgesetzt sind, die aus zirkulierendem und lokal abgelagertem Triacylglycerin stammen, wird die glukosevermittelte Insulinsekretion unterdrückt. Die Insulinresistenz beschleunigt das Fortschreiten der Fettleber, wobei ektopische Fettablagerungen in Leber und Betazellen eine zentrale Rolle bei der Insulinresistenz und Betazelldysfunktion spielen. Der Verzehr einer hyperkalorischen Ernährung, reich an gesättigten Fetten, hängt, im Rahmen eines genetischen Hintergrunds, kausal mit der Entstehung von Typ-2-Diabetes zusammen.
(3/4) Nutritional investigation of non-obese patients with non-alcoholic fatty liver disease: the significance of dietary cholesterol
2008: Cholesterin oxidiert und reguliert damit Rezeptoren, die die Leber verfetten lassen.
Association between dietary nutrient composition and the incidence of cirrhosis or liver cancer in the United States population
2009: 13 Jahre an 9000 beobachtet: Cholesterin oxidiert im Körper und verursacht toxische und karzinogene Effekte. Cholesterineinnahme korreliert stark mit Leberzirrhose und Leberkrebs.
NLRP3 inflamasomes are required for atherogenesis and activated by cholesterol crystals
2010: Cholesterin sorgt dafür, dass weiße Blutkörperchen entzündliche Stoffe ausscheiden.
The role of diet and nutrient composition in nonalcoholic Fatty liver disease
2011: Eine nicht-alkoholische Fettleber ist die häufigste Lebererkrankung, steht in engem Zusammenhang mit der Insulinresistenz, gilt als hepatische Manifestation des metabolischen Syndroms und ist die Ursache für weitere chronische Lebererkrankungen.
Molecular mechanisms and the role of saturated fatty acids in the progression of non-alcoholic fatty liver disease
2012: Gesättigte Fettsäuren haben sich als besonders toxisch für die Leberzellen erwiesen, die eine Fettlebererkrankung verursachen. Wenn man menschlichen Leberzellen pflanzlichen Fettsäuren aussetzt, passiert nichts. Wenn man Leberzellen tierischen Fettsäuren aussetzt, stirbt ein Drittel von ihnen. Zahlreiche Studien haben gezeigt, dass gesättigte Fettsäuren toxischer sind als ihre ungesättigten Pendants, was zu einer progressiven lipotoxischen Kaskade führt. Abbildung 1: Gesättigte Fettsäuren lösen eine zelluläre Dysfunktion bei Lipotoxizität/NAFLD aus.
Hepatic cholesterol crystals and crown-like structures distinguish NASH from simple steatosis
2013: Freies Cholesterin akkumuliert in verfetteten Leberzellen, kristallisiert dort und führt zu Leber-Entzündungen (Hepatitis).
The Gordian Knot of dysbiosis, obesity and NAFLD
2013: Wenn man Fett isst, füttert man die schlechten Bakterien im Darm, die Entzündungen fördern und zu einem durchlässigen Darm (Leaky Gut) beitragen. Dadurch wird das angeborene Abwehrsystem in der Leber aktiviert und die Leber nimmt Schaden auf zellulärer Ebene. Abbildung 2: Umweltfaktoren wie Nahrungsfette können bei einer nicht-alkoholischen Fettleber eine Dysbiose auslösen und die Durchlässigkeit des Darms erhöhen. Dieser Schritt führt zur Verlagerung von pathogen-assoziierten molekularen Mustern wie Lipopolysaccharid, die Toll-like-Rezeptoren auf verschiedenen Leberzellpopulationen aktivieren können. Es wird angenommen, dass die Aktivierung von Toll-like-Rezeptoren auf Kupffer-Zellen eine Entzündung auslöst, und die Aktivierung von Toll-like-Rezeptoren auf stellative Leberzellen stimuliert die Fibrose.
Non-high-density lipoprotein cholesterol independently predicts new onset of non-alcoholic fatty liver disease
2013: Um sich von der toxischen Wirkung von Cholesterin zu schützen, schüttet der Körper das Cholesterin ins Blut aus, somit kann man mit dem Messen des non-HDL-Cholesterins schätzen wie verfettet die Leber ist. Keine Patienten mit einem non-HDL-Cholesterin von kleiner als 130 mg/dl entwickelten eine nicht-alkoholische Fettleber.
Cholesterol-induced non-alcoholic fatty liver disease and atherosclerosis aggravated by systemic inflammation
2014: Cholesterin lagert sich nicht nur in der Arterien ab, sondern auch in der Leber.
(4/4) Wie Typ 1 Diabetes entsteht
Intakte tierische Aminosäuren kommen hauptsächlich durch eine durchlässige Darmwand (Leaky Gut Ursachen) ins Blut, die durch Alkohol, gesättigte Fettsäuren, Cholesterin und schlechte Darmbakterien durch Tierprodukte und Antibiotika entsteht. Antikörper werden von den Lymphozyten gesendet, um die tierischen Aminosäuren anzugreifen, und lösen dabei eine molekulare Mimikry aus. Dabei kopieren die tierischen Aminosäuren die Aminosäurestruktur der Betazellen, sodass die Antikörper nun nicht nur die tierischen Aminosäuren im Blut, sondern auch die Betazellen der Bauchspeicheldrüse als Feind erkennen und zerstören.
A bovine albumin peptide as a possible trigger of insulin-dependent diabetes mellitus
1992: Das Casein aus der Kuhmilch hat genau die gleichen 17 Aminosäuren wie die Betazellen unserer Bauchspeicheldrüse. Alle Diabetiker hatten erhöhte Serumkonzentrationen von IgG-Anti-BSA-Antikörpern und IgA-Antikörpern. Patienten mit insulinabhängigem Diabetes mellitus haben eine Immunität gegen Kuhmilchalbumin, mit Antikörpern gegen ein Albuminpeptid, das mit einem Betazell-spezifischen Oberflächenprotein reagieren kann. Solche Antikörper können an der Entwicklung einer Inseldysfunktion beteiligt sein.
Diet, cow's milk protein antibodies and the risk of IDDM in Finnish children. Childhood Diabetes in Finland Study Group
1994: Die frühe Einführung von Milchprodukten und ein hoher Milchkonsum in der Kindheit erhöhen die Kuhmilch-Antikörperspiegel und sind mit hohen IgA-Antikörpern gegen Kuhmilch-Formula, unabhängig voneinander, mit einem erhöhten Typ-1-Diabetes-Risiko verbunden.
Cell-mediated immune response to beta casein in recent-onset insulin-dependent diabetes: implications for disease pathogenesis
1996: Eine spezifische Proliferation von T-Lymphozyten mit Rinder-Beta-Casein wurde bei Patienten mit Typ 1 Diabetes festgestellt. Der Zusammenhang zwischen Typ 1 Diabetes und einem frühem Kuhmilchkonsum lässt sich möglicherweise durch die Entstehung einer spezifischen Immunantwort auf Beta-Casein erklären. Die Exposition gegenüber Kuhmilch löst eine zelluläre und humorale Anti-Beta-Casein-Immunantwort aus, die mit einem Betazell-Antigen kreuzreagieren kann. Es gibt Sequenzhomologien zwischen Beta-Casein und mehreren Betazell-Molekülen.
Preservation of beta-cell function in type 1 diabetes
1999: Typ 1 Diabetes wird durch eine autoimmune Zerstörung der Betazellen verursacht, die bereits Jahre vor der vollständigen Zerstörung der Betazellen einsetzt. Der frühe Kontakt zu Kuhmilch wurde als umweltbedingter Auslöser für die autoimmune Zerstörung der Betazellen identifiziert.
Whole cow's milk in infancy
2003: Kuhmilchproteine erhöhen bei Säuglingen das Risiko, eine Allergie gegen Milchproteine zu entwickeln. Wegen des möglichen Zusammenhangs zu Typ 1 Diabetes wird in Familien mit einer starken Vorgeschichte dringend empfohlen zu stillen und handelsübliche Kuhmilch und Produkte, die intaktes Kuhmilchprotein enthalten, im ersten Lebensjahr zu meiden.
Antibody cross-reactivity between myelin oligodendrocyte glycoprotein and the milk protein butyrophilin in multiple sclerosis
2004: Bei Tierversuchen wurde gezeigt, dass Milchprotein eine Autoimmunreaktion auslösen kann. Die Lymphozyten können Antikörper produzieren die sowohl das Milchprotein als auch die Myelinscheiden angreifen. Dadurch sterben auch die Nerven im Gehirn ab und man entwickelt Multiple Sklerose.
Dr. John McDougall über Autoimmunerkrankungen allgemein:
"Arthritis ist weder eine Erbkrankheit noch ein unvermeidlicher Teil des Älterwerdens. Es gibt Ursachen für diese Gelenkbeschwerden, und sie liegen in unserer Umwelt. Unser engster Kontakt mit unserer Umwelt ist unsere Nahrung. Einige Forscher glauben, dass rheumatoide Arthritis vor 1800 nirgendwo auf der Welt existierte (1). Es ist gut dokumentiert, dass diese Formen der Arthritis in der ländlichen Bevölkerung Asiens und Afrikas früher selten bis gar nicht vorkamen (2,3,4). Noch 1957 wurde in Afrika kein Fall von rheumatoider Arthritis gefunden. Zu dieser Zeit ernährten sich die Menschen in Afrika noch von Getreide und Gemüse. Den ersten Fall von Lupus in Afrika gab es 1960. Diese einstmals unbekannten Gelenkerkrankungen treten nun immer häufiger auf, da die Menschen in wohlhabendere Länder auswandern oder in die Großstädte ihrer Heimatländer ziehen. Mit diesen Veränderungen haben sie ihre traditionelle Ernährung mit Getreide und Gemüse zugunsten von Fleisch, Milchprodukten und stark verarbeiteten Lebensmitteln aufgegeben, wodurch die Häufigkeit von rheumatoider Arthritis in Dritte-Welt-Ländern weiter steigt (5,6,7). So sind zum Beispiel Afroamerikaner in den USA führend in der Häufigkeit von Lupus, obwohl dies vor 1960 in Afrika unbekannt war (8,9). Die Mechanismen, durch die eine ungesunde Ernährung eine entzündliche Arthritis hervorruft, sind komplex und kaum erforscht, betreffen aber unseren Darm und unser Immunsystem."
Soviel Aufwand für so wenig Fakten. Eine Ansammlung von Falschaussagen und völlig falschen Schlussfolgerungen.
Die Quellen, die du verwendest, stützen deine Aussagen gar nicht. Aber sowas ist typisch, wenn die (falsche) Meinung schon vorher feststeht und man krampfhaft nach Quellen googelt und sich an alles klammern muss.