Welchen Einfluss haben die Kohlensäureformen auf das Kalk-Kohlensäure-Gleichgewicht?
Hallo zusammen,
ich muss demnächst ein Referat über die Auswirkungen des pH-Wertes auf das Kalk-Kohlensäure-Gleichgewicht halten. Ich habe auch schon einige grundlegende Sachen zu dem Thema herausgefunden, beispielsweise weiß ich das der Kalk in saurem Wasser gelöst wird. In alkalischem Wasser bilden sich hingegen Kalkablagerungen. Allerdings hat mir mein Lehrer zur Unterstützung ein Arbeitsblatt gegeben, das mir bei der Recherche helfen soll. Dabei geht es um Kohlensäureformen. Ich habe dazu herausgefunden, daß es drei Kohlensäureformen gibt, die je nach pH-Wert unterschiedlich stark ausgeprägt sind, bspw. ist bei einem hohen pH-Wert viel CO3^2- im Wasser, wenig HCO3^ und fast kein CO2. Meine Frage wäre nun, welche Auswirkungen die Anteile der jeweiligen Kohlensäureformen auf das Kalk-Kohlensäure-Gleichgewicht haben. Was hat das mit meinem eigentlichen Thema zu tun?
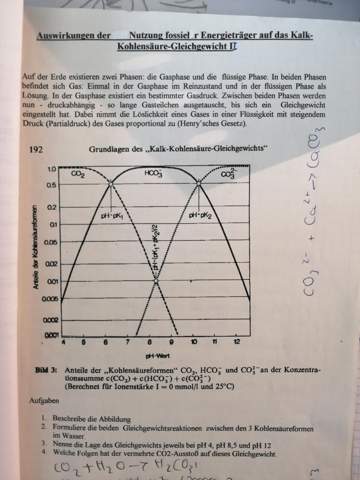
Das ist das Arbeitsblatt, das mein Lehrer mir zur Hilfe gegeben hat.
Schonmal vielen Dank vorab 🙏
LG Sandelholz
1 Antwort
Möglicherweise bezieht sich der Unterschied darauf, dass "Kohlendioxid im Wasser" noch nicht "Kohlensäure" ist. Kohlendioxid löst sich nämlich im Wasser, auch ohne damit eine chemische Verbindung einzugehen. Unter Druck bleibt es dann überwiegend im gelösten, aber nicht chemisch gebundenem Zustand.
Das, was oft "Kohlensäure" genannt wird, ist zum Großteil nur in Wasser gelöstes Kohlendioxid, erkennbar am größeren CO2 Gehalt des Wassers.