Redoxgleichungen von Nebengruppen?
Hallo,
ich soll eine Redoxgleichung aufstellen von dem Metall Fe(s) in der Metallsalz-Lösung ZnSO4. Ich habe kleinen Plan, wie man die Reduktion und die Oxidation darstellen soll.(Unter anderem, weil Eisen in der Nebengruppe steht )
1 Antwort
Hallo Marie
Bei Redoxreaktionen kommt es grundsätzlich nicht draufan, ob ein Element in der Nebengruppe steht oder nicht. Wichtig zu wissen ist, welcher Stoff Elektronen abgibt, und welcher sie aufnimmt. Dazu gibt es die Elektrochemische Spannungsreihe (Redoxreihe).
Bei deiner Reaktion reagiert festes Eisen mit Zn2+. Nun kannst du in der Redoxreihe nachschauen, wo diese Stoffe stehen. Du siehst, dass Fe zwei Elektronen abgibt, und Zn2+ zwei Elektronen aufnimmt.
Oxidation bedeutet Elektronenabgabe. Also ist die Reaktion von Eisen zu Eisen 2+ eine Oxidation.
Reduktion bedeutet Elektronenaufnahme. Also ist die Reaktion von Zn2+ zu Zn eine Reduktion.
Für die Redoxgleichung stellt man zuerst die beiden so genannten Teilgleichungen auf, eine für die Oxidation und eine für die Reduktion. Wenn man diese Teilgleichungen zusammenfügt erhält man die Redoxreaktionsgleichung.
Hier noch ein Bild:
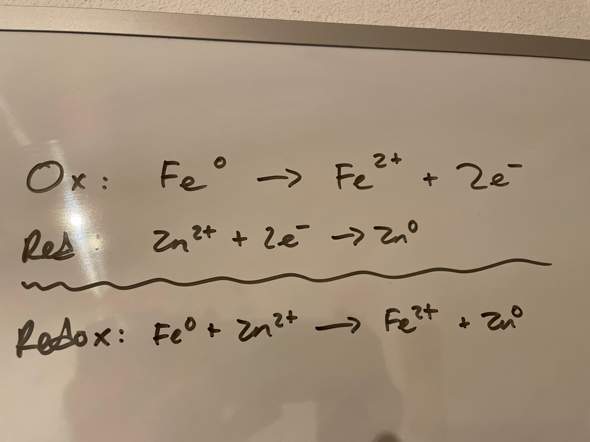
Grüsse, Fabio
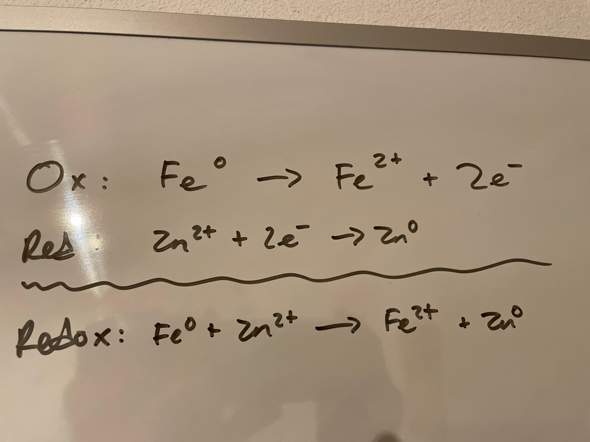
Sehr gern geschehen! Die sollte bestimmt irgendwo in deinem Chemiebuch oder Skript sein, weil sie so wichtig ist. Sonst hier ein Link zu einer Onlineversion: https://www.chemie.de/lexikon/Elektrochemische_Spannungsreihe.html
Grundsätzlich kann Eisen 1, 2 oder sogar 3 e- abgeben. Du findest alle diese Halbreaktionen in der Redoxreihe. Die Reaktion, bei der Eisen 2e- abgibt ist 6 Zeilen unter der fett markierten Wasserstoffreaktion.
Eisen gibt so viele Elektronen ab, wie es energetisch am günstigsten ist. Das kann man an diesen Zahlen rechts neben der Halbreaktion sehen.
Schon Mal vielen lieben Dank!!!! Woher finde ich die redoxreihe ?