Oxidationzahl bestimmen?
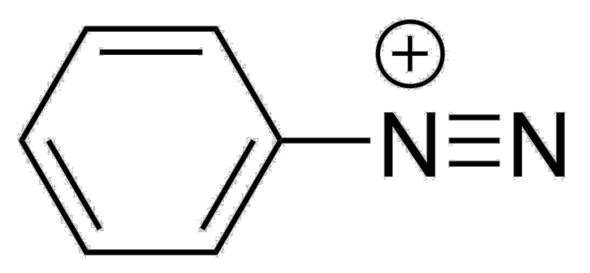
Meine Frage ist, welche Oxidationzahl hat das positiv geladene Stickstoff Atom?
Normalerweise schaue ich immer die Bindungspartner an und zähle je nach elektronegativität die Elektronen.
In dem Fall drei Elektronen mit Stickstoff da beide gleich stark ziehen jeweils 3 und nochmal 2 Elektronen mit aus der Einfachbindung mit dem Kohlenstoff somit 5 dann wäre die Oxidationszahl aber 0 wie kann das mit der positiven Ladung übereinstimmen?
1 Antwort

Du hast richtig gerechnet — Oxidationszahlen und Formalladung haben nichts miteinander zu tun, sie sind unterschiedliche Möglichkeiten, wie man die Elektronen den Atomen zuordnet. Deshalb ist ihre Summe über alle Atome dieselbe, nämlich die Ladung des Moleküls (die Aufteilung ändert ja nichts an der Anzahl der Elektronen), aber da enden die Gemeinsamkeiten.
Anderes Beispiel: Im H₃O⁺ hat O die Formalladung +1 und die Oxidationszahl −II.

Dann verwendest Du also ein modifiziertes Verfahren, die Elektronen den Atomen zuzuordnen. Das kann man natürlich machen, aber was dabei herauskommt, ist dann nicht mehr die handelsübliche Oxidationszahl.

Elektronegativität ist ein Kompromiss zwischen Elektronenaffinität und Ionisierungsenergie. Beide Größen kann man messen, und beide Größen sind definiert. Elektronegativität und Oxidationszahl sind Begriffe aus dem Übergang der Alchimie zur echten Chemie als exakter Naturwissenschaft.
FALSCH! Da ein positiviertes Atom gegenüber einem neutralen Atom desselben Elements die größere Elektronegativität hat. -3 wäre hier formal richtig.