Maßanalytisches Äquivalent?
Hi, weiß jemand wie man auf 26,1 mg kommt? Ich weiß, dass man m= (0,1M * 0,001L * 783 g/mol * z(Mslg)) : z(Analyten) rechnen muss. Wie kommt man auf z vom Analyten hier?

2 Antworten
Chininsulfat enthält 2 Moleküle chinin und einmal Schwefelsäure. Ein Molekül Chinin kann je 2 Protonen aufnehmen: also insgesamt 4. Da Schwefelsäure aber auch protoniert sind insgesamt nur 3 protonierbare Stellen noch frei. Hydrogensulfat wird mit Perchlorsäure nicht protoniert. Daher ist der Verbrauch 3 mol Perchlorsäure für 1 mol Chininsulfat.
PS: hab dann (0,1 * 0,001 * 783)÷3 gerechnet
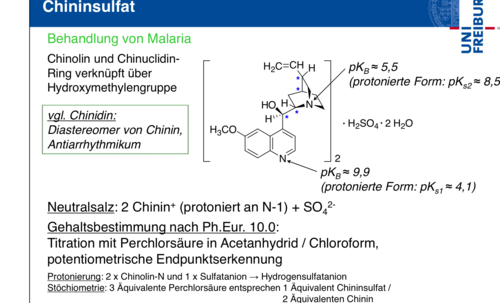
Das hier habe ich zu dem Thema gefunden:

So recht habe ich das nicht verstanden, denn schließlich gibt es in einem mol Chininsulfat prinzipiell 4 titrierbare basische Zentren. Aber ich habe auch keine Erfahrung mit der Rechnerei bei wasserfreien Titrationen. Vielleicht kann ein Kollege vom Fach hier noch Erleuchtendes beitragen. 3 Äquivalente Perchlorsäure entsprechen demnach einem Äquivalent Chininsulfat = 2 Äquivalente Chinin.