Lewis Schreibweise, 3D Anordnung- gewinkelt oder linear?
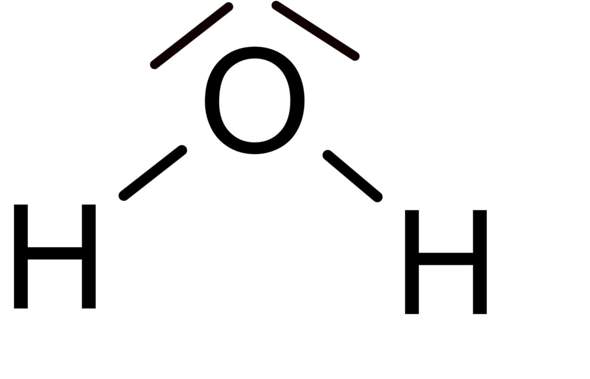
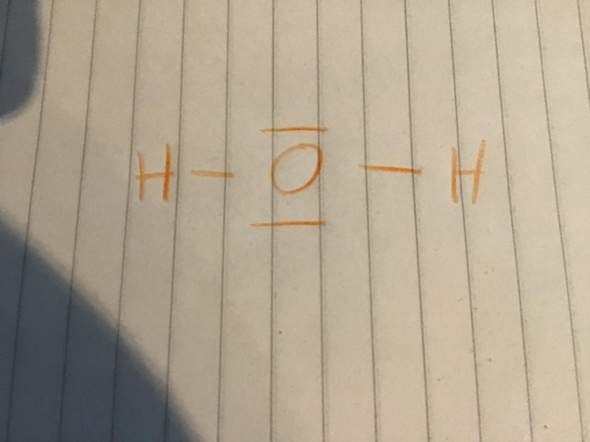
Hallo. Habe eine Frage zur 3 dimensionalen Anordnung der Atome in einer Atombindung. Bsp.: H20 ist in der Lewis schreibweise ja in etwa wie in Bild 1. Aber wieso nicht linear wie in Bild 2? Die beiden freien Elektronenpaare haben trotztem Platz und sind so weit wie möglich von den anderen Elektronenpaaren entfernt (innerhalb vom Radius). Also warum gewinkelt? Hat es vielleicht auch was mit der eigentlich tetraedischen Struktur zu tun (bei Mitbetrachtung der freien Elektronenpaare)?
2 Antworten
Linear entstehen 90° Winkel zu den freien Elektronenpaaren, in der 3. Dimension, im Tetraeder aber 109,48°, was also fast 20° MEHR Platz ist.
Achso ok danke. Diese 2D Schreibweise obwohl es eigentlich 3D ist verwirrt mich xD habs mir am vom Schreiben der Frage irgendwie gedacht dass es was mit dem 2D-3D Zusammenhang zu tun hat
Ja, das Stichwort ist „Tetraeder“ — wenn sich vier „Dinger“ (egal ob Bindungen oder freie Elektronenpaare) um ein Zentralatom drängen, dann nehmen sie eine tetraedrische Konfiguration ein. Es ist auch leicht zu sehen, warum das so ist: Dann haben sie nämlich mehr Platz. In Deinem hypothetischen linearen H₂O hätte jedes von den vier „Dingern“ zwei andere im 90-Grad-Abstand, in einem Tetraeder gibt es aber Abstände von 109 Grad, also weiter weg.