Ionenbildung im Modell?
Hallo ,
Ich schreibe morgen eine Chemie Arbeit und habe ein übungsblatt gefunden zu dem Thema aber verstehe es nicht weiß jemand die Lösung ?
Danke für jede hilfreiche Antwort :)

2 Antworten
Hallo princes345
Atome versuchen in einer Verbindung eine möglichst stabile Konfiguration zu erreichen und das ist die Edelgaskonfiguration/Oktett.
Treffen nun Atome mit einer niedrigen Elektronegativität (EN) und einer hohen EN zusammen, so bilden sie eine Ionenbindung.
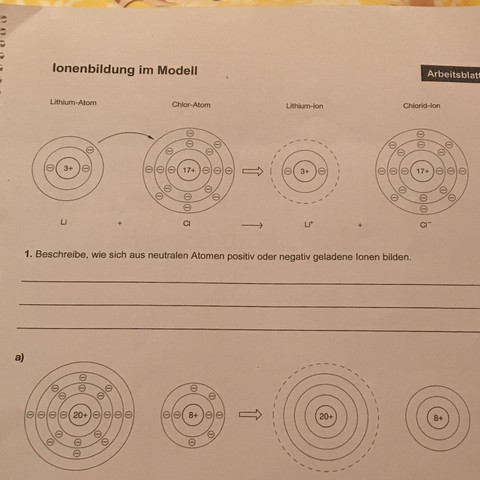
In deinem ersten Beispiel hat Li die EN: 1.0 und Cl die EN 3.2. Die Differenz der EN ist mit 2.2 hoch. Das Li-Atom erreicht nun sein Oktett, indem es sein einziges Außenelektron dem Chloratom vollständig überlässt. So entstehen positive Li-Kationen Li^+ und negative Cl-Anionen Cl^-.
In deinem zweiten Beispiel handelt es sich um Ca mit der Ordnungszahl 20 und der EN: 1.0 sowie O mit der Ordnungszahl 8 und der EN: 3.4. Das Calcium erlangt nun sein Oktett, indem es seine zwei Außenelektronen ganz zum Sauerstoff verlagert. So entstehen Ca^2+ und O^2-.
Im dritten Beispiel verbindet sich Magnesium (Ordnungszahl: 12 und EN: 1.3) mit zwei Fluoratomen (Ordnungszahl: 9 und EN: 4.0). Die beiden Fluoratome bekommen je ein Außenelektron des Mg. Es entstehen die Ionen Mg^2+ und 2 mal F^-.
LG
Hallo!
Also für den Test morgen bist Du jetzt eigentlich schon reichlich spät dran...
Sieh Dir mal Lehr-Videos auf Youtube an:
Das Atommodell nach Bohr:
https://www.youtube.com/results?search_query=atommodell+bohr
Und für die Zeit nach dem Test: Das Orbital-Atommodell:
https://www.youtube.com/results?search_query=atommodell+orbitale
Es gibt sehr viele lehrreiche Videos zu den Naturwissenschaften.
Gruss,
Martin