Die Lewis Formel anhand der Oktettregel ist doch so richtig ausgeführt, oder?
Guten Abend
Ist die Lewis-Formel anhand der Oktettregel richtig benutzt ?
Ich freue mich auf eure Antworten.
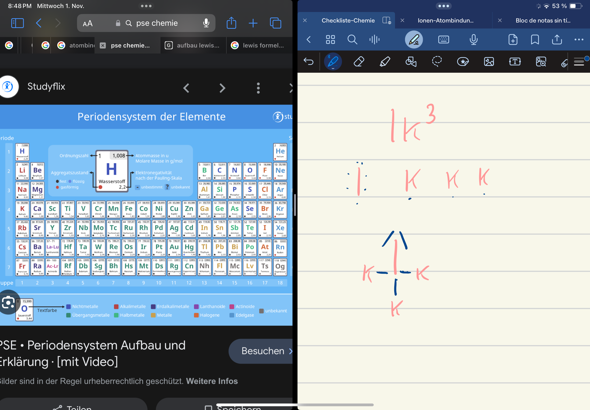

Soll das Kaliumiodid werden?

ja
2 Antworten

Kalium befindet sich in der ersten Hauptgruppe und bildet in gewöhnlichen chemischen Verbindungen Kationen K^+. Iod in Gruppe 17 erhält durch Aufnahme eines Elektrons ein Oktett, bildet also I^-. Die Reaktion lautet also 2 K+ I2 -> 2 KI. Das ist eine ionische Verbindung, keine mit kovalenten Bindungen. Eine Lewisformel anzugeben, ergibt also keinen rechten Sinn.

Da gibt es nur die Ionenschreibweise. K-I-Moleküle gibt es in Kaliumiodid nicht.

Kaliumiodid ist ein Salz. Da kann man keine Lewis-Formel angeben, das geht nur bei Molekülen.
Die Formel von Kaliumiodid ist KI, nicht KI3.
Die 3 müsste, falls sie richtig wäre, tiefgestellt sein.
Was soll ich dann machen?
Wie stelle ich Ionenbindungen dann da?
Wie unterscheide ich sie zu Atombindungen?