Kann mir jemand diese Lewis Formel erklären?
Hallo! Ich versteh diese Lewis Formel nicht. Würde das nicht bedeuten, wenn sich die Elemente kein EP teilen, dass sie nicht verbunden sind?
Danke im Voraus
1 Antwort
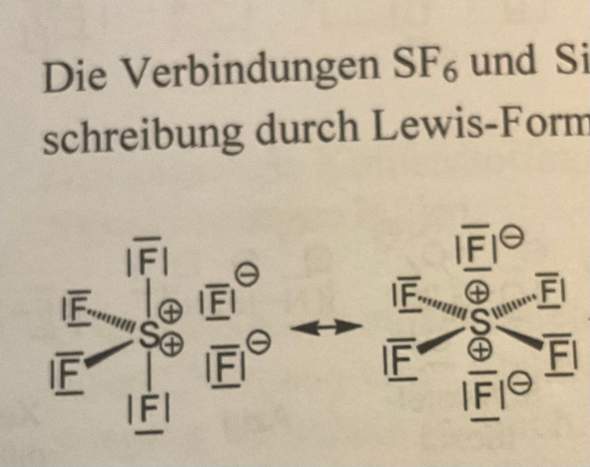
Auf dem Bild sind zwei Lewis-Strukturen für SF₆, Schwefelhexafluorid, zu sehen. In einer Lewis-Struktur repräsentieren die Punkte Valenzelektronen und Striche Elektronenpaare, die Atome miteinander teilen. Bei SF₆ teilt Schwefel seine Elektronen mit sechs Fluoratomen, um sechs S-F-Bindungen zu bilden. Jedes Fluoratom hat drei nichtbindende Elektronenpaare, die als Punkte dargestellt sind, und teilt ein Elektronenpaar mit Schwefel (dargestellt als Strich). Schwefel ist im Zentrum mit einer oktaedrischen Geometrie. Die Darstellung suggeriert eine Resonanzstruktur, aber das ist hier nicht korrekt, weil alle S-F-Bindungen identisch sind; SF₆ ist ein Molekül mit sechs gleichen Schwefel-Fluor-Bindungen.
Es sind "Momentaufnahmen" die durch die Regeln der Lewis-Schreibweise bedingt sind. Sie sind nicht real. Zudem ist die Darstellung nicht vollständig.
Danke für die Antwort! Was soll diese Lewis Formel dann bedeuten?