Chemie Übungsaufgaben hilfe?
Ich habe hier einige Übungsaufgaben und bräuchte Hilfe dabei. Leider fällt mir Chemie unglaublich schwer und würde mich über jede Hilfe freuen. Es bringt leider auch nichts dann das falsche zu üben wenn man es nicht verstanden hat.
Ich bedanke mich im Voraus.
4 Antworten
Das ja richtiges Ü Ei. In der Tat sehr gute Übungsaufgaben... Du wirst viel dabei lernen, wenn Du dir das alles selber erarbeitest. Es geht hier um das Element Magnesium.
a) Elektronen, 12, Atomhülle, negativ | Protonen, 12, Atomkern, positiv | Neutronen, variabel je nach Isotop, Atomkern, neutral.
b) Ja
c) Isotopen unterscheiden sich in der Anzahl der Neutronen, Das chemische Verhalten wird hauptsächlich von der Atomhülle also den Elektronen bestimmt.
d)
e) Eine Elementfamilie haben ähnliche Eigenschaften. Magnesium gehört zu den Erdalkalimetallen.
Vielen lieben Dank, die Antwort ist super und hilft mir weiter beim lernen :) dann weiß ich jetzt wo ich dran bin und kann üben ohne mir sorgen zu machen alles falsch verstanden zu haben.
Danke. Mein Dank gilt auch an die Kollegen, die die gleichen Aufgaben ganz toll gelöst haben.
Magnesium besteht aus 12 Elektronen,12 Protonen und 12 Neutronen.
Magnesium gehört zur 2.Hauptgruppe, auch Erdalkalimetalle genannt.
Magnesium gehört wie alle Metalle zu den Kationen,d.h das es positiv geladen ist.
Ladung kann aber,ohne dass das Magnesium eine Verbindung eingeht,auch neutral sein.
Beim schalenmodell :
1.Schale: 2. Elektronen
2.Schale: 8. Elektronen
3.Schale: 2. Elektronen
c) 26 u ist ein radioaktives Magnesium Isotop,d. h der Kern hat 2 Neutronen mehr,als Protonen.
d) 2• n ^2(Hoch 2) =18
e) Wo diese häufig auftreten,Magnesium gehört zu den erdalkalimetallen
Aufgabe 4:
a)
Proton | 12 | Atomkern | +
Elektron | 12 | Atomhülle | -
Neutron | (26 - 12) 14 | Atomkern | 0
b)

(https://www.lernhelfer.de/sites/default/files/lexicon/article_image/BWS-CHE-PSE-e012c.gif)
c)
Isotope sind Atome, welche sich hinsichtlich ihrer Neutronenzahl (aber nicht Protonenzahl!!!) unterscheiden und somit auch unterschiedliche Atommassen aufweisen.
Das chemische Verhalten von Isotopen ist weitgehend gleich.
Manche sind instabil und zerfallen halt nach einer gewissen Zeit.
Man benötigt halt minimal mehr Energie, da wir auch mehr Masse haben, aber sonst würde mir nichts direktes mehr in den Sinn kommen.
d)
Die Formel lautet:
Das heißt, dass die 3. Schale maximal 18 Elektronen aufnehmen kann.
e)
Magnesium gehört zur Elementfamilie der Erdalkalimetall (2. Hauptgruppe).
Die Kennzeichen einer Elementfamilie sind zudem annähernd gleiche Eigenschaften.
Zum Beispiel sind die Erdalkalimetalle äußerst reaktiv und haben allesamt 2 Valenzelektronen.
~Johannes.
Hallo TheTimeLove
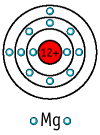
Magnesium steht in der 2. Hauptgruppe in der dritten Periode und hat die Ordnungszahl 12. Diese Ordnungszahl 12 ist gleich der Anzahl der positiven Protonen im Kern und bei einem ungeladenen Atom gleich der Anzahl negativer Elektronen in der Hülle. Hinzu kommen im Kern 12 bis 14 neutrale Neutronen - je nach Isotop, wobei 12 die weitaus häufigste Neutronenzahl ist.
Zum Schalenmodell vielleicht ein Bild:
https://upload.wikimedia.org/wikipedia/commons/6/67/12_magnesium_(Mg)_Bohr_model.png
isotope habe ich schon angesprochen. Verschiedene Isotope unterscheiden sich nur in der Anzahl ihrer Neutronen. Da an chemischen Reaktionen nur die Elektronen beteiligt sind, bleibt das chemische Verhalten davon unbeeinflusst.
Für die maximale Aufnahmefähigkeit von Elektronen in den Schalen gilt: x = 2 n²
Somit kann die 1. Schale 2 Elektronen, die 2. Schale 8 Elektronen, die 3. Schale 18 Elektronen usw. aufnehmen.
Im Periodensystem sind Elemente mit ähnlichen Eigenschaften in Gruppen eingeteilt, dies gilt insbesondere für die 1., 2., 7. und 8. Hauptgruppe. Magnesium steht zusammen mit Be, Ca, Sr und Ba in der zweiten Hauptgruppe. Diese Elemente werden als Erdalkalimetalle bezeichnet.
LG
Vielen Dank für die unglaublich hilfreiche Antwort :)
Du siehst man kann das schaffen, alle anderen hier sind genau auf die gleichen Antworten gekommen.