Bau und Wirkungsweise von Enzymen
Chemische Reaktionen benötigen zum optimalen Ablauf spezifische Temperaturen, die wir in der Zelle nicht immer vorfinden. Ist die Bedingung einer optimalen Temperatur nicht gegeben, laufen Reaktionen nicht oder nur sehr langsam ab. Es entsteht eine Art Barriere, die man Aktivierungsenergie nennt. Erhöht man die Temperatur und damit die Energiezufuhr, wird diese Barriere überwunden. Hier kommt die sogenannte RGT-Regel (Reaktions-Geschwindigkeits-Temperatur-Regel) zum tragen, die besagt, dass mit einer Erhöhung der Temperatur um 10 °C die Reaktionsgeschwindigkeit verdoppelt oder gar verdreifacht werden kann.Bei Stoffwechselreaktionen wird auch eine Aktivierungsenergie benötigt, die jedoch nicht durch eine Erhöhung der Temperatur überwunden werden kann, da diese die Zellen möglicherweise schädigt oder abtötet. Bei Proteinen sorgt eine zu hohe Temperatur für eine Denaturierung, d.h. die Proteine werden fest und können nicht mehr in ihren Ausgangszustand zurückkehren. Dieser Vorgang ist irreversibel. Dieser Prozess ist vergleichbar mit einem Ei, das gekocht wurde und anschließend nicht wieder verflüssigt werden kann. Aus diesem Grund benötigen die Zellen andere Katalysatoren (=Beschleuniger), die für einen schnellen Ablauf chemischer Reaktionen sorgen: die Enzyme. Enzyme beschleunigen selektiv (=auswählend) Stoffwechselreaktionen, indem sie die Aktivierungsenergie herabsetzen und damit die Reaktionsgeschwindigkeit erhöhen. Dies ermöglicht den Ablauf chemischer Reaktionen bei in der Zelle herrschenden Temperaturen. Abb. 1 zeigt eine exotherme Reaktion, d.h. eine Reaktion, bei der Energie frei wird, mit und ohne Katalysator.Neben der Temperatur spielt auch der pH-Wert eine wichtige Rolle bei Stoffwechselvorgängen. Enzyme bevorzugen meist einen pH-Wert von 7, um chemische Reaktionen beschleunigen zu können. Einige Enzyme können aber auch in Milieus mit extremen pH-Werten die Aktivierungsenergie herabsetzen und so Reaktionen beschleunigen. Ein Beispiel hierfür sind die bei einem pH-Wert von 2 im Magen arbeitenden Enzyme.
Der Verlauf einer enzymatischen Reaktion
Enzyme weisen häufig eine für Proteine typische, komplizierte räumliche Struktur auf. Für die Katalyse (= Beschleunigung) einer enzymatischen Reaktion spielt nur eine Teilregion des Proteins eine wichtige Rolle: das aktive Zentrum. Das aktive Zentrum kann man sich als vertiefte Tasche vorstellen, in die sich ein Substrat, also das umzusetzende Molekül, setzt. Durch diese Bindung entsteht ein Enzym-Substrat-Komplex.Nicht jedes Substrat kann eine Bindung mit einem beliebigen aktiven Zentrum eingehen, sondern die Bindung erfolgt nach dem Schlüssel-Schloss-Prinzip. Diese Eigenschaft wird als Substrat- spezifität bezeichnet.
Hallo, ich hab mir den Text zu der Abbildung durchgelesen aber verstehe noch immer nicht wie ich die Abbildung zu deuten habe. Könnt ihr mir helfen ? :)
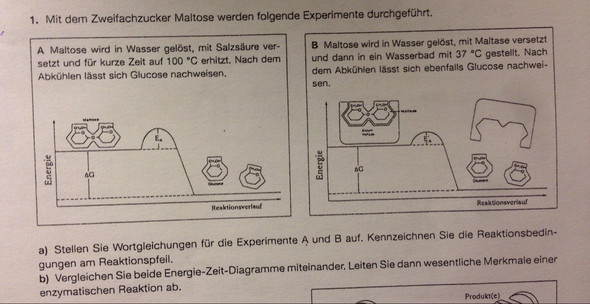
Dankeschön ;)