
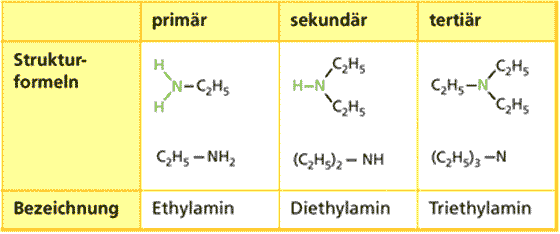
Bei primären Aminen ist das Stickstoff Atom an ein C-Atom gebunden, bei sekundären an zwei und tertiären an drei C-Atome.
Die basische Wirkung von Aminen ergibt sich aus dem freien Elektronenpaar am Stickstoff über das ein Proton gebunden werden kann.
Die Alkylreste (die C-Atome mit allem was dranhängt) haben einen elektronenschiebenden Effekt (+I Effekt) und erhöhen dadurch die Elektronendichte am N-Atom wodurch dieses leichter Protoniert werden kann.
Damit gilt grundsätzlich für die Basizität:
Primär < Sekundär < Tertiär
Allerdings spielt in wässriger Lösung auch der Hydratisierungsgrad eine Rolle. In der Realität ist die Reihenfolge daher meist eher:
Tertiär < Primär < Sekundär
Allerdings gilt diese Reihung nur innerhalb einer Klasse (in diesem Fall aliphatische Amine). Je nach Substituenten kann die Basizität sehr unterschiedlich sein.







