Probleme in Chemie (Thema: Alkohole und Molmasse) Wie geht das:?
Hallo alle bin gerade richtig verzweifelt und weiß nicht was ich machen soll... Wir haben für eine Klausur Übungsaufgaben bekommen jedoch war ich in der letzten Woche Krankheitsbedingt nicht da. Zwei Aufgaben verstehe ich leider gar nicht! Die erste:
Bestimmen sie die Masse folgender Alkohole
a: Methano------b: Ethanol------c: 2 Heptanol usw.
Wie zum Teufel soll man das machen ich meine wie soll man denn die molare Masse herausfinden wenn man nicht die Stoffmenge hat.
Zweite Aufgabe:
Berechnen sie Anhand dieser Reaktionsgleichung: C6 H12 O6 (Glucose ) ->(Hefe beimischung) -> 2C2 H5 OH + 2CO2 (alkoholische Gärung) nach bekanten Dreischritt aus welche Masse an Glucose (Zucker) um unter idealen Bedingungen 10g reinen Ethanol zu bekommen.
Wie soll das bitte gehen? Zum Dreischritt aus Aufgabe 2 habe ich diesen Artikel gefunden: http://onlinelibrary.wiley.com/doi/10.1002/ckon.19940010305/abstract;jsessionid=A981DC7A38E2D743B70B62DFA3E5DC05.f02t01
Hoffe ihr könnt mir helfen. Verzweifel und will wirklich keine schlechte Note in der Klausur ...
Danke im Vorraus.
2 Antworten
Die molare Masse ist stoffmengenunabhängig, bzw. ist es die Masse von einem Mol. Sie wird in g/mol angegeben und, wenn man denn eine konkrete Stoffmenge hat, mit dieser multipliziert.
Für die Gärungsaufgabe:
Molare Masse von Ethanol bestimmen, ausrechnen wieviel Mol 10 g Ethanol sind.
Aus der Rk.Gl. weißt du, dass ein Mol(ekül) Glucose zu zwei Mol(ekülen) Ethanol wird.
Dementsprechend brauchst du also für x mol Ethanol ½x mol Glucose. Das rechnest du dann mit der molaren Masse von Glucose in g Glucose um.
Ja, wenn man das mit den Molen mal verstanden hat, ist das sehr simpel.
Schön, dass du es verstanden hast.
Teil 1 - Berechnung der Molmasse
Die Molmasse ist so etwas wie ein Umrechnungsfaktor zwischen Masse (=Gewicht = m [g]) und der Stoffmenge (=Teilchenzahl = n [mol]).
Du kannst die Molmasse eines jeden Stoffes mit Hilfe des Periodensystems ausrechnen, wenn du seine Formel kennst. Machen wir das mal am Beispiel des Ethanols:
1. Formel rausfinden: Etanol = C2H5OH
2. Nun suchst du dir die Massen der Atome im Periodensystem raus:
C: 12g/mol
H: 1g/mol
O: 16g/moll
3. Zusammenaddieren:
C + C + H + H + H + H + H + O + H
=
12 + 12 + 1 + 1 + 1 + 1 + 1 + 16 + 1 = 46[g/mol]
Soweit alles klar?
_________________________________________________________
Diese Zahl 46[g/mol] ist die Molmasse und damit der Umrechnungsfaktor. Du musst nun die folgenden beiden Formeln kennen:
n [mol] = m[g] / M [g/mol]
m [g] = n [mol] * M [g/mol]
Diese beiden Formeln sind quasi ein Fahrstuhl, um im folgenden zweiten Teil zwischen der "n-Zeile" und der "m-Zeile" hoch und runter zu fahren.
____________________________________________________________
Teil 2 - Rechnen mit Stoffmengen und Reaktionsgleichungen.
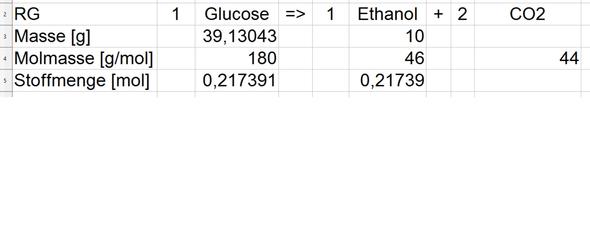
Schau dir, bevor du diese Schritte liest, das Bild zu meiner Antwort an.
1. Reaktionsgleichung aufschreiben und unter jedes Molekül eine Spalte machen.
2. Unter die Reaktionsgleichungen 3 Zeilen schreiben. Eine für die Stoffmenge, eine für die Molmasse, eine für die Masse.
3. Für alle Moleküle die Molmassen berechnen (Wie das geht, steht oben) und in ihre Zeile eintragen.
4. Alles eintragen, was du bis dahin weißt. Das ist bis dahin nur die Masse von Ethanol.
5. Über die erste der beiden Formeln die Stoffmenge(n) von Ethanol ausrechnen und in ihr Feld eintragen. Das ist hier 0,21739.
6. Jetzt kommt der spannende Teil, den in der Stoffmengen-Zeile darf man auch von Links nach rechts übertragen und zwar genau in dem Verhältnis, wie es die die stöchiometrischen Koeffizienten in der Reaktionsgleichung beschreiben. Lange Rede, kurzer Sinn: Weil bei Ethanol und Glucose dieselbe Zahl davorsteht (eine 1), muss auch bei der Stoffmenge von Glucose eine 0,21739 stehen. (Bei der Stoffmenge von CO2 müsste das Doppelte stehen - also 0,436...)
7) Nun kommt der letzte Schritt: Du rechnest mit der anderen Fahrstuhl-Formel von Stoffmenge Glucose wieder auf die Masse an Glucose. Und da kommt dann 39,1g raus.
8) FERTIG
=> Probier es aus. Dieses System funktioniert immer.
LG
MCX
Danke schonmal! Ich habe es glaube ich verstanden!!! Ich glaube es hat klick gemacht und es kommt mir sehr einfach vor... Wie konnte ich nur so etwas fragen ?! *:* Danke!