Lewis-Struktur vom sulfation?
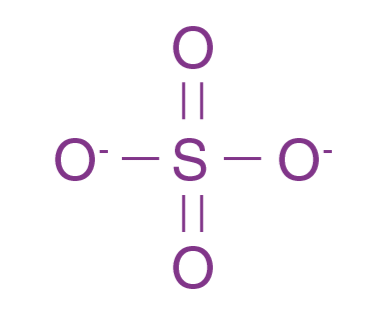
Folgendes: Die Atome sollen ja so gut wie möglich die Edelgaskonfiguration erreichen und die O-Atome haben ja in der Abbildung mit den geteilten Elektronen insgesamt 8 Elektronen. Aber das Schwefel-Atom hätte ja dann laut der Abbildung nur 12 Elektronen oder? Kann mir einer erklären wie das mit der Edelgaskonfiguration zusammenpasst?
1 Antwort
Stell dir vor am Ende jedes Striches ist je 1 Punkt (•-• , so ungefähr).
Ein Punkt ist dabei ein Elektron.
Ein Punkt gehört dann dem Sauerstoff und das andere dem Schwefel.
Wenn also eine Verbindung entsteht teilen sich die Arome also die Elektronen.
Ja, das weiß ich natürlich schon. Aber das erklärt leider nicht meine Frage. Am Ende schaut es tritzdem so aus, als würde das Schwefelatom 12 Elektronen gleichzeitig mit anderen O-Atomen teilen.