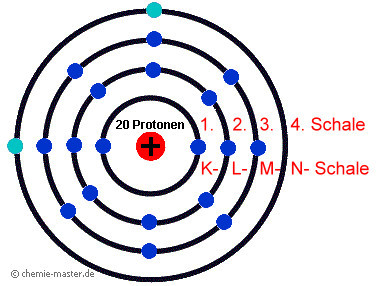
Schalenmodell M?
auf der M-Schale haben ja max. 18 elektronen platz... warum sind es dann hier nur 8?
Bitte eine einfache Erklärung :) danke
2 Antworten
Ich kann dir es versuchen anhand der Elektronenkonfiguration erklären. Es gibt keine Hauptschalen, sondern nur Unterschalen dieser nach Energieniveaus. Die Besetzung erfolgt nach Energie durch die Bank.
Die Unterschalen heißen s, p, d, f, g, h für jede Hauptschale. K hat nur s, L s und p, M s, p und d. s nimmt 2 Elektronen maximal auf, p 6, d 10... man nennt K-s zB auch 1s-Orbital usw mit L, M, N. Die EK für Calcium hieße (2, 8, 8, 2 Elektronen) 1s2, 2s2, 2p6 (2s+2p(L)=8), 3s2, 3p6 (M=8), 4s2 ( Valenzhauptschale).
Die M-Schale wird nach Energie mit Scandium (21) mit 2, 8, 9, 2 weiter besetzt, weiter bei Titan mit 2, 8, 10, 2. Bis 4p, dauert es, bis 3d6 bzw das ganze M-Orbital voll ist.
Hoffe man versteht es, einfacher geht es nicht :) das kommt auch nur im Chemie-Lk dran.
Im Unterricht habe ich gelernt das auf der äußersten Schale nur 8 Elektronen Platz haben, dementsprechend keine Ahnung wo du die Zahl 16 her hast
*18 E(z)=2*z^2 wobei E die Gesamtzahl der maximalen Elektronenbesetzung einer Schale und z die Schalenzahl ist. Daher 18. Sollte man wissen.